Kuidas diabeet areneb? Mis põhjustab suhkurtõbe: miks see juhtub täiskasvanutel ja lastel, põhjused
Selle kahjuks Venemaal levinud haiguse magus nimi tõotab selle omanikule väga magusat elu. Diabeedi kohta on kirjutatud sadu lehekülgi õpikuid ja see artikkel esitab erinevatest allikatest pärit sünteesitud materjali, mis vastab põhilistele diabeediga seotud küsimustele.
Mis on suhkurtõbi?
Suhkurtõbi on haigus, mille korral patsientidel on häiritud glükoosi assimilatsiooniprotsess organismis, selle rikkumise tagajärjeks on hormooninsuliini täielik või osaline puudulikkus. Glükoosi imendumise ja keharakkudesse sisenemise eest vastutab insuliin, kui protsess on häiritud, siseneb glükoos vereringesse.
Maailmas kannatab umbes 415 miljonit inimest (Venemaa Diabeediassotsiatsiooni andmed), kuid ainult 50% neist on oma haigusest teadlikud.
Diabeedi leviku kiirus on kohutav, juhtumite arv kahekordistub iga kümnendiga. Seega on 2026. aastaks see näitaja miljardi lähedal. Seetõttu toimub tänapäeval populariseerimine õige toitumine tarbitud suhkru koguse vähendamine, tervislik eluviis elu. Kõik need meetmed vähendavad selle haiguse tekke riski.
Arvamus, et diabeet on suhkrut sisaldavate toitude tohutu tarbimise tõttu meie aja haigus, on ekslik, kuna seda tunti juba 3. sajandil eKr. Vanad roomlased, kreeklased ja egiptlased suutsid seda haigust tuvastada, kirjeldada, kuid nad ei leidnud viisi selle raviks.

Diabeedi sümptomid ja tunnused
Nagu iga haiguse puhul, on ka diabeedil mitmeid iseloomulikke tunnuseid. Kuid nende olemasolu võib märgata juba pärast haiguse arengut, esimesed etapid võivad olla asümptomaatilised.
Diabeedi peamised nähud naistel ja meestel:
- sagedane tung urineerida
- pidev janu
- kaalukaotus
- üldine nõrkus ja väsimus
- pearinglus
- vähenenud nägemine
- krambid
- jäsemete tuimus
Enamikku muid sümptomeid peale janu ja sagedase urineerimise võib seostada vanuse, ilma, väsimuse ja stressiga. Seetõttu juba ägenemisega arsti poole pöördudes selgub, et diabeet on juba välja kujunenud.

Esimesed diabeedi tunnused
Erilist tähelepanu tuleks pöörata esimeste sümptomite tuvastamisele ja nende hoolikale ravile. Glükoosi taseme tõusu tõttu, mida organism ei suutnud veres töödelda, peavad neerud selle kehast eemaldamiseks kõvasti tööd tegema. Siit ka sage urineerimine ja pidev janutunne, sest vaja on kaotatud vedelikku täiendada. Nõiaring viib neeru- ja maksahaigustega seotud tüsistusteni.

Diabeedi tüübid
Üldine klassifikatsioon sisaldab 4 peamist diabeedi tüüpi:
- Diabeet esiteks tüüp
Pankreas, mis vastutab insuliini tootmise eest, lõpetab selle tootmise või vähendab selle kogust. Selle tulemusena suureneb glükoosi sisaldus veres ja uriinis.
- Diabeet teiseks tüüp
2. tüüpi diabeedi korral toodetakse insuliini normaalselt, kuid glükoos ei saa siiski rakku siseneda ja jääb verre, see tähendab, et rakud muutuvad insuliini suhtes tundetuks.
- Rasedusaegne diabeet
Rasedusdiabeet võib ilmneda ainult rasedatel naistel, seda diagnoositakse 24-26 rasedusnädalal, see on seotud üldise muutusega. hormonaalne taust. Pankreas toodab muutustega toimetulemiseks kolm korda rohkem insuliini, samal ajal kui kolmandal trimestril hakkab ka platsenta oma hormoone tootma. Platsenta hormoonid blokeerivad raseda naise insuliini ja põhjustavad diabeedi.
- muud sordid:
- diabeedi geneetilised vormid;
- Pankrease haigused;
- Diabeet, mis on põhjustatud kõhunäärme talitlust mõjutavate ravimite võtmisest;
- Suhkurtõbi, mis on põhjustatud kõhunäärme talitlust kahjustavast nakkushaigusest.

Diabeedi arengu põhjused
Endokrinoloogid nimetavad mitmeid diabeedi tüübist sõltuvaid põhjuseid, mis võivad olla haiguse arengu lähtepunktiks.
1. tüüpi diabeet
I tüüpi suhkurtõbi tekib 90% juhtudest geneetilise eelsoodumuse tõttu. Seetõttu on arsti esimene küsimus teie perekonna ja sugulaste diabeedi esinemise kohta. Samal ajal, kui ühel vanematest oli diabeet, on risk haigestuda palju väiksem.
Arstid esitavad järgmised arvud: pärilikkus edastatakse 5% juhtudest emaliini kaudu ja 10% isaliini kaudu, samas kui haigus diagnoositakse mõlemal, suureneb selle edasikandumise oht 70% -ni.
Ja ometi ei tohiks see kõlada lausena, diabeedi tekkimine algab kindlal põhjusel, näiteks haiguse või süsivesikuterikka dieedi tõttu. Dieedi ja geneetilise eelsoodumusega saate elada terve elu ja ei tea, mis on diabeet.
2. tüüpi diabeet
2. tüüpi diabeet on kõige levinum, selle peamised põhjused on:
- Ülekaaluline ja suur hulk rasvkude
- Ebaõige toitumine
- pidev stress
- Istuv ja istuv eluviis
Tavaliselt on ohus üle 50-aastased naised, mistõttu on oluline läbida pidevad uuringud.
Rasedusdiabeet
Selle esinemise põhjus seisneb muutustes, mis toimuvad naise kehas raseduse arenguga. Seda tüüpi diabeeti esineb vaid 3-5% naistest.
Muud tüüpi diabeet
Nende arengu põhjuseks võivad olla kõhunäärme geneetilised kõrvalekalded või operatsioon, infektsioonid, mis mõjutavad selle tööd. Pankreatiit, kasvajad või vigastused võivad samuti põhjustada diabeedi arengut.

Mis põhjustab diabeeti?
Olenemata suhkurtõve tüübist on liigne suhkrutarbimine peamine põhjus, mis vallandab haiguse arengu. Kaasaegsed tootjad lisavad suhkrut peaaegu kõikidele toitudele, nii et te tõesti ei kujuta ette, kui palju suhkrut päevas tarbite.
Suhkrut sisaldavad jogurtid, kiirpüreed ja teraviljad, leib, majonees, vorstid, mahlad, kohupiim ja isegi dieetleivad. Mõned tootjad varjavad suhkrut, asendades selle melassi, maisisiirupi vms, kuid tulemust see ei muuda.
Arstide soovituste kohaselt ei tohiks naine tarbida rohkem kui 6 supilusikatäit suhkrut päevas. Näiteks klaasis viinamarjamahlas on 4 supilusikatäit suhkrut, see tähendab, et teie päevane norm on poolteist klaasi mahla. Väikeses soodapurgis on 8-10 supilusikatäit suhkrut.

Diabeedi tekkimise oht
Diabeedi tekkerisk on kindlasti suurem inimestel, kelle sugulastel on alla 50-aastased, kellel on see haigus tekkinud. Kuid ärge lõõgastuge, kui seda haigust teie ajaloos pole. Istuv eluviis, suhkrut sisaldavate toitude suurem tarbimine võib viia II tüüpi diabeedi tekkeni.

Diabeedi arengut soodustavad tegurid
Diabeedi tekke tõenäosust mõjutavad peamised tegurid on järgmised:
- pärilik suhkurtõbi
Vanematelt saadud geneetiline materjal on keeruline kromosoomide komplekt. Tõenäosus haigestuda ühelt vanemalt on palju väiksem kui mõlemalt korraga. Tasub kohe mainida, et jutt käib alla 50-aastaste täiskasvanute haigustest, vanematel inimestel areneb see haigus pigem vanuse kui geneetiliste põhjuste tõttu.
- Viiruslikud haigused
Teadlased räägivad mumpsi ja punetiste viiruste vahelisest seosest ning sellele järgnevast diabeedi tekkest. Samuti on mitmeid uuringuid, mis kirjeldavad diabeedi juhtumeid imikutel, kelle emadel oli raseduse ajal punetisi.
- Sagedased stressirohked olukorrad
Glükoos vastutab energia eest ning stressi ajal kulub energia väga kiiresti ära, toiduks ei jätku aega ning võib tekkida hüpoglükeemiline seisund, mis viib I tüüpi diabeedini.
- arteriaalne hüpertensioon
Kõrge vererõhk on ka üks diabeedi väljakujunemise tegureid. Need kaks haigust on omavahel niivõrd seotud, et põhjustavad heaolu pidevat halvenemist.

Diabeedi testid
Selle haiguse täpseks tuvastamiseks on vaja läbida mitmeid teste, sealhulgas:
- Vere glükoosisisaldus
Analüüs võetakse hommikul tühja kõhuga, söömine tuleks lõpetada 12 tundi enne analüüsi, siis on tulemus usaldusväärne. Tervetel inimestel on veresuhkru tase alla 5,1 mmol / l.
- Glükoosi taluvuse test
Tavaliselt on see test ette nähtud rasedusdiabeedi tuvastamiseks. Analüüsi tegemiseks kulub 2 tundi, esmalt loovutatakse verd tühja kõhuga, seejärel juuakse siirupit 75 g vees lahjendatud glükoosist. Arvatakse, et see suhkruannus võrdub suure koogitükiga. Ebameeldiva maitse vähendamiseks on lubatud juua väike kogus sidrunimahla.
Seejärel võetakse kontrollnäit 1 tunni ja 2 tunni pärast pärast siirupi võtmist. Saadud kolme arvu (tühja kõhuga, 1 tunni pärast ja 2 tunni pärast) võrreldakse normiga, tühja kõhuga on norm alla 5,1 mmol / l, ülejäänud numbrid peaksid olema alla 7,8 mmol / l. Diabeedi diagnoos tehakse, kui teine indikaator ületab 10 mmol / l. Analüüsi uuesti ei tehta, seega olge esitamisel ettevaatlik.

- Glükeeritud hemoglobiini analüüs: tulemuseks on suhkurtõbi
See indikaator on üks usaldusväärsemaid, see peegeldab veresuhkru taset protsentides st kui suur osa hemoglobiinist on seotud glükoosiga. Glükomeetritega mõõdetud veresuhkru tase peegeldab glükoosi olemasolu enne või pärast sööki, samas kui seeduvus on individuaalne omadus. Seetõttu on glükosüülitud hemoglobiini analüüs mitmekülgsem. Tulemus üle 5 mmol / l näitab prediabeedi või diabeedi olemasolu.
- Glükoosi tase uriinis
Analüüs kogutakse ka hommikul spetsiaalsesse konteinerisse. Tavaliselt ei tohiks glükoos uriinis olla, see tähendab, et keha peaks selle täielikult omastama. Mõnel juhul võib arst paluda teil teha igapäevane uriinianalüüs, peate koguma kogu päeva uriini suurde purki ja registreerima, kui palju vedelikku olete selle aja jooksul joonud. Seejärel mõõtke purki kogunenud maht ja andke analüüsiks väike kogus uriini, valades see anumasse.
- Analüüs ketokehade esinemise kohta uriinis
Ketoonkehade tase määratakse indikaatoritega testribade abil. Sellist testi saate teha kodus, terve inimese norm on kuni 20-50 mg päevas. Suurenenud ketoonkehade sisaldus viitab alatoitumisele ja maksa talitlushäiretele.

Diabeedi areng
Erinevat tüüpi suhkurtõve areng toimub erinevatel stsenaariumidel:
- 1. tüüpi diabeet
- Diabeedi tekkimise võimaluse eest vastutavate defektsete geenide olemasolu.
- Haiguse areng alatoitluse, stressi, infektsiooni tõttu.
- Toodetud insuliinikoguse vähenemine, sümptomid ei ilmne 2-3 aasta jooksul.
- Väsimus, halb enesetunne, tolerantse diabeedi teke.
- Janu ja sagedane urineerimine, suur ja kiire kaalulangus on selged diabeedi sümptomid.

- 2. tüüpi diabeet
- Haiguse areng alatoitluse taustal.
- Esimeste sümptomite ilmnemine, mis on seotud janu ja kehakaalu langusega, kõrge veresuhkur.
- Suhkru taseme korrigeerimine dieedi abil.
- Suhkrutaseme korrigeerimine dieedi ja suhkrut langetavate ravimitega.
- Suhkrutaseme korrigeerimine dieedi, suhkrusisaldust langetavate ravimite ja insuliinisüstidega.
Hüvitise etapid:
- Kompenseeritud diabeet, näitajad korraliku ravi korral on normilähedased.
- Subkompenseeritud diabeet, mõõdukas haiguse kulg, sümptomite suurenemine.
- Dekompenseeritud suhkurtõbi, väga suur tüsistuste risk ( südame-veresoonkonna süsteemist, neerud, maks, nägemine).
- Rasedusdiabeet
Rasedusdiabeet areneb 24-26 rasedusnädalal, see tähendab kolmanda trimestri alguses. Sellel on üks põhietapp, mis kestab kolm kuud kuni sünnituseni. Veresuhkru tõusu on oluline kompenseerida dieediga ja pideva suhkrutaseme jälgimisega.
Muud tüüpi diabeet areneb vastavalt individuaalsele stsenaariumile, sõltuvalt haiguse põhjusest.

Mida teha, kui teil on diagnoositud diabeet?
Kahjuks on suhkurtõbi krooniline haigus, mis nõuab kohustuslikku ravi. Selle ees ei saa silmi kinni pigistada ja loota, et kõik läheb iseenesest. Kõige rohkem varajased staadiumid peate järgima ainult dieeti, raskematel juhtudel on vaja ravi.

Kuidas diabeeti ravida?
Erinevat tüüpi diabeeti ravitakse erineval viisil:
Diabeedi ravi esiteks tüüp
I tüüpi diabeeti nimetatakse ka insuliinist sõltuvaks, kuna insuliini toodetakse tavapärasest vähem. Põhimõtteliselt on ravi süstid, annus arvutatakse individuaalselt. Glükomeetri näitude põhjal süstib patsient puuduoleva ravimiannuse.
Õige arvutus väldib hüpokleeemiat, st puudumist või üleannustamist. Dieet vähendab süstide arvu, vähendades glükoositarbimist, ja trenn põletab ära kõik ülejäägid.
Diabeedi ravi teiseks tüüp
2. tüüpi diabeet on tavaliselt seotud alatoitumise ja liigsete kilodega. Endokrinoloog peab hindama kehamassiindeksit (KMI) – see näitaja võrdub inimese kehakaalu kilogrammides jagatud pikkusega meetrites ruudus.

Näiteks kui kaal on 80 kg ja pikkus on 1,5 m, jagame 80 / (1,5) 2 \u003d 35,6 \u003d KMI. Tavaliselt peaks see näitaja naistel olema 19–24.
Tavaliselt algab ravi madala kalorsusega dieediga, mis sisaldab vähe kiireid süsivesikuid ja loeb leivaühikuid. Kui ühest dieedist ei piisa, lisage diabeedi ravimid nagu Novonorm, Metformin jt. Järgmine etapp seisneb lisaks põhiravile insuliinisüstide lisamises.
Ravi rasedusaegne diabeet
Rasedusdiabeet ravitakse ilma arstide sekkumiseta pärast sünnitust, kui kõik muutused naise kehas on normaliseerunud. Paljud arstid nõuavad vere glükoosisisalduse määramiseks läbivaatust 3-6 kuud pärast sünnitust. Arvatakse, et rasedusdiabeedi avaldumine suurendab tulevikus diabeedi tekkeriski.
Ravi teised diabeedi tüübid
Teiste diabeeditüüpide ravi seisneb selle arengu põhjuse väljaselgitamises ja vajaliku insuliinikoguse kompenseerimises süstide või ravimitega.

insuliin diabeedi jaoks
Iga kolmas diabeetik on sunnitud tegema insuliinisüste. Nende kasutamise sageduse tõttu on vaja hirmust üle saada ja õppida neid iseseisvalt kasutama:
- Nõel torgatakse nahaalusesse rasvkoesse, et otse vajalikku piirkonda sattuda, tuleb nahka ja nahaalust rasvakihti pigistada, moodustades nahavoldi.
- Nõela pikkus sõltub patsiendi suurusest ja süstekohtadest.
- Lühikesed, kõigest 4-5 mm nõelad sobivad süstimiseks jäsemetel nahavolti, pikemad kõhu- ja reiesse süstimiseks.
- Väikesed nõelad sisestatakse 90-kraadise nurga all, pikad 45-kraadise nurga all.
Tasub tähelepanu pöörata alaline vahetus insuliini süstekohtadesse, nii väldite lipodüstroofiat ja punnide teket pideva süstimise kohtades.
Tavaliselt süstitakse:
- kõht
- tuharad
- õla pehmed kuded
- reie pehmed kuded
Diabeetikute võimalike manustamisvõimaluste hulgas on ohutuma ja valutuma süstimist võimaldavate süstlanõelte või tavaliste süstalde kasutamine. Iga uue süsti jaoks on soovitatav kasutada uut nõela. Diabeedi ravi on paraku üsna kulukas pideva ravimite ja tarvikute vajaduse tõttu.

Glükomeeter diabeedi jaoks
Diabeetikute kohustuslik seade on taskuglükomeeter, mis võimaldab mõne sekundiga hinnata veresuhkru taset. Seadmed on varustatud kobestitega naha hõlpsaks punktsiooniks. Hindamisprotseduur koosneb järgmisest toimingute jadast:
- Sisestage mõõturisse uus testriba
- Torgake kobestiga sõrme nahk läbi
- Eemaldage esimene tilk vatitikuga
- Vajutage oma sõrme alla, et moodustada teine veretilk
- Tooge testriba
- Mõne sekundi pärast hinnake tulemust
Diabeetikute norm on suhkru tase tühja kõhuga 5–7,2 mmol / l pärast söömist alla 10 mmol / l.
Torkekohtade puhul kasutatakse tavaliselt sõrmeotste külgi. Haav paraneb väga kiiresti ja mõne tunni pärast pole seda enam näha. Glükomeetri kasutamine on väga mugav ja võimaldab kiiresti hinnata suhkru taset. Ainus negatiivne külg on kulumaterjalide üsna kõrge hind. 50 testriba maksavad umbes 800-1000 rubla, asenduslansetid skarifikaatorile umbes 200 rubla 50 tk. Mõlemad vajavad pärast iga mõõtmist väljavahetamist. Päevas on vaja 4-5 testi.

Mida diabeediga inimesed söövad?
Diabeedi dieet ei ole ainult piiratud toitude kogum ja madala kalorsusega toitude valik, vaid ka teatud miinimum- ja maksimumpiirid tarbitavate süsivesikute osas. Vajaliku ööpäevase süsivesikute koguse hindamiseks võtsid arstid kasutusele mõiste "leivaühik" (1XE), ühes leivaühikus on umbes 12 g süsivesikuid ning kõiki tooteid mõõdeti neis sisalduvate leivaühikute arvu järgi.
Päevamäär diabeetik 18-25 XE päevas, võib vähenemine või suurenemine põhjustada ketokehade ilmnemist uriinis.
Sa pead sööma 3-5 korda päevas, väikeste portsjonitena. Korraldage söögikordi iga 3-4 tunni järel, tarbige korraga 4-6 XE-d. Kui võrrelda konkreetsete näidetega, siis
- 1 XE:
- 1 klaas piima
- tükk leiba
- 1 lusikas granuleeritud suhkrut
- supilusikatäis jahu

- 2 XE
- 100 grammi jäätist
- 4 tassi õunamahla
- 2 klaasi kalja või õlut
- 400 grammi vorsti
- 2 kotletti
Diabeetik peab täpselt teadma, kui palju leivaühikuid tarbitud toiduained sisaldavad, et hinnata päevanormi. See tähendab, et võite süüa maiustusi, kuid sisse piiratud koguses. Diabeediga nädala menüü peaks sisaldama mitmesuguseid vitamiinirikkaid ja aeglaseid süsivesikuid sisaldavaid toite.
Samuti on oluline hinnata toiduainete glükeemilist indeksit, see on see näitaja, mis vastutab toiduainete lagunemise kiiruse, see tähendab glükoosi kehasse sisenemise ja selle kontsentratsiooni suurendamise kiiruse eest. Sellised hüpped mõjuvad halvasti diabeedihaigete tervisele. Seetõttu tuleb kõrge glükeemilise indeksiga toiduainetega olla ettevaatlik.
Diabeedile ohtlike kõrge glükeemilise indeksiga toiduainete loetelu:

Korduma kippuvad küsimused diabeedi toitumise kohta
Peamiste muret tekitavate küsimuste hulgas:
- Kas diabeediga on võimalik alkoholi juua?
Alkoholil on kahjulik mõju isegi tervete inimeste kehale, seetõttu on parem hoiduda alkohoolsete jookide võtmisest. Kui te ei saa seda endale lubada, siis on parem valida kangete jookide hulgast (üle 40 kraadi), need sisaldavad vähem suhkrut kui veinid, liköörid ja šampanja. Mõned teadlased räägivad õllepärmi teatud eelistest, kuid joodud õlle kogus peaks mahtuma lubatud leivaühikutesse.
- Kas on võimalik kasutada mett diabeediga?
Mesi sisaldab oma koostises lihtsuhkruid (glükoos ja fruktoos), lubatud on 1-2 supilusikatäit mett päevas.
- Kas diabeediga on võimalik õunu süüa?
Madal glükeemiline indeks, kõrge vitamiinisisaldus, minimaalne süsivesikute kogus teevad õunad üheks ohutumaks toiduaineks. Arvatakse, et kõige parem on süüa küpsetatud õunu, kuumtöötlemise tõttu kaob osa glükoosist ja kõik kasulikud omadused jäävad alles.
- Kas diabeediga on võimalik fruktoosi sisaldavat toitu süüa?
Fruktoosi peetakse kaks korda magusamaks kui suhkrut, seedimine võtab kauem aega ja sellel on madal glükeemiline indeks. Võimaldab kuni 30 g fruktoosi päevas diabeeti põdevatele inimestele. Küpsetistes fruktoosi kasutamisel tasub meeles pidada selle suurenenud magusust.

Diabeedi tüsistused ja keerulised haigused
Suhkurtõbi põhjustab kehas mitmeid muutusi, mis põhjustavad teiste haiguste arengut või ägenemist:
- Kõrge vererõhk diabeedi korral. Diabeedi tekkega on hüpertensiooni risk kõrge, kombinatsioonis diabeediga püsib rõhk pidevalt kõrgel tasemel, ei vähene isegi öösel. Sellistel juhtudel on vajalik pidev jälgimine ning suhkru ja soola tarbimise piiramine.
- Madal vererõhk diabeedi korral. Suhkurtõbi mõjutab südame tööd, mis ei suuda tagada normaalset survet. Madal vererõhk põhjustab diabeedi arengut ja edasi nõiaringi. Soovitatav on arsti järelevalve ja kontrastdušš, massaaž, roheline tee.

- Troofilised haavandid. Arstid on moodustanud eraldi mõiste "diabeetiline jalg", mis tähendab kuivi kontsi ja lõhesid, mida ei saa eemaldada. Nende esinemise põhjuseks on väikeste veresoonte ja närvilõpmete kahjustus ning kuna jalad on südamest kõige kaugemal, algab protsess nendega. Troofiline haavand on naha sügav defekt, mis tekib kapillaaride kahjustuse tagajärjel.
- Ainevahetushaigus. Kompenseerimata suhkurtõbi põhjustab erinevaid ainevahetushäireid, üheks ilmseks sümptomiks on ülekaalulisus. Sisemiselt toimuvad muutused märkamatult, kuid enamikul diabeetikutel diagnoositakse maksa rasvumine, süsivesikute, vee, valkude ja mineraalide ainevahetuse rikkumine.
- Suhkurtõbi ja kilpnäärme talitlushäired. Harvadel juhtudel võivad kilpnäärmehaigused provotseerida suhkurtõve teket, tavaliselt juhtub vastupidi, ainevahetushäired mõjutavad näärme talitlust. Eksperdid jälgivad omavahelist seost autoimmuunhaigus kilpnääre ja 1. tüüpi diabeet.

Diabeedi vastunäidustused
Diabeetikutel on rangelt keelatud dieedi rikkumine ja insuliini süstide vahelejätmine, kuna mõlemad toimingud võivad põhjustada haiguse ägenemist. Suhkrust loobumine on väga raske, sest see tekitab sõltuvust. Kuid mõne nädala pärast tunnete ka ise muutusi, meeleolukõikumised mööduvad, hommikul on kergem tõusta, avastate uuesti tuttava toidu maitse.

Mis on diabeedi jaoks hea?
Treening on eriti kasulik diabeetikutele. Sport aitab vabaneda rasvumisest ja normaliseerida ainevahetust. Harjutus on suurepärane glükoosi põletamiseks.
Saate valida ühe järgmistest programmidest:
- Füsioteraapia. Seda soovitatakse liigse kehakaalu all kannatavatele inimestele, see võimaldab koormust järk-järgult tõsta, keha ette valmistada tõsisteks jõuharjutusteks. Kohapeal kõndimine, kükid, painutused – kõiki neid lihtsaid harjutusi saab teha kodus.
- Jooga. Need tegevused võimaldavad teil lõõgastuda, kõrvale juhtida mõtteid tervisest ning leida sisemist energiat, tasakaalu ja jõudu haigusega võitlemiseks.
- Hiina võimlemine Tai chi. See võimlemine ühendab tantsu ja võitlustehnika elemendid. Lihtsad harjutused ei vaja koolitust ja saate neid hõlpsalt ise teha.
- Matkamine. Rasedad, kes ei saa aktiivselt spordiga tegeleda, peaksid kindlasti pühendama matkamisele 1-1,5 tundi päevas.

Diabeedi ennetamine
Isegi peres diabeediga inimesed saavad seda haigust vältida, kui nad juhivad õiget elustiili, keelduvad ülesöömisest ja kõrge kalorsusega toidust. Samuti on oluline märkida, et võtmise ajal peate pidevalt jälgima oma veresuhkru taset iga-aastased uuringud spetsialistidelt.

Tänapäeval on kõik reklaamid täis ahvatlevaid pakkumisi diabeedi kiireks raviks. Petturid kasutavad meile tuntud staaride nägusid, teenides raha kellegi teise haiguse pealt. Kahjuks pole suhkurtõbe ravida, see on krooniline haigus, mis jääb elu lõpuni. Kuidas te end tunnete ja selle haigusega leppite, kui see teie uksele koputab, on teie otsustada.
Miljonid inimesed elavad jätkuvalt täisväärtuslikku elu, tööd, lõõgastuda ja reisida, kõik samad laiad võimalused on Sulle avatud nagu varemgi, ainus piirang toidus ei tohiks muuta Sinu ülejäänud elu. Hoolitse enda eest ja ole terve!
Video: suhkurtõbi: ravi rahvapäraste ravimitega
Diabeet- organismi insuliinipuudusest põhjustatud haigus, mis põhjustab tõsiseid süsivesikute ainevahetuse häireid, aga ka muid ainevahetushäireid.
Suhkurtõbi on haigus, mida iseloomustab insuliini ebapiisava toime tõttu kõrge veresuhkru tase. Insuliin on hormoon, mida eritab kõhunääre, täpsemalt Langerhansi saarekeste beeta-rakud. Suhkurtõve korral puuduvad need täielikult või on insuliinsõltuv diabeet või keharakud ei reageeri sellele piisavalt (või insuliinisõltumatu diabeet). Insuliin reguleerib ainevahetust, eelkõige süsivesikuid (suhkruid), samuti rasvu ja valke. Suhkurtõve korral tekib insuliini ebapiisava kokkupuute tõttu keeruline ainevahetushäire, veresuhkru taseme tõus (hüperglükeemia), suhkur eritub uriiniga (glükosuuria), happelised rasvapõlemisproduktid - ketoonkehad (ketoatsidoos). veri.
Diabeedi peamised tunnused on tugev janu, sagedane urineerimine koos suure koguse uriiniga ja mõnikord dehüdratsioon (dehüdratsioon). Mõned 1. ja 2. tüüpi diabeedi sümptomid on erinevad.
Diabeedi diagnoosimine
 Diabeedi diagnoos tehakse vere suhkrusisalduse (glükeemia) analüüsi põhjal, vaidlustatud juhtudel pärast glükoosi manustamist. Kui patsiendil on (janu, tugev urineerimine, näljatunne või kaalulangus), piisab veresuhkru analüüsist. Kui selle tase on kõrgenenud, on tegemist suhkurtõvega. Kui patsiendil puuduvad diabeedile omased sümptomid, kuid on vaid suhkurtõve kahtlus, tehakse glükoositaluvuse test, mille põhimõte on kirjeldatud eespool. Organismi reaktsioon sellele koormusele määrab, kas tegemist on tõesti suhkurtõvega või ainult glükoositaluvuse häirega.
Diabeedi diagnoos tehakse vere suhkrusisalduse (glükeemia) analüüsi põhjal, vaidlustatud juhtudel pärast glükoosi manustamist. Kui patsiendil on (janu, tugev urineerimine, näljatunne või kaalulangus), piisab veresuhkru analüüsist. Kui selle tase on kõrgenenud, on tegemist suhkurtõvega. Kui patsiendil puuduvad diabeedile omased sümptomid, kuid on vaid suhkurtõve kahtlus, tehakse glükoositaluvuse test, mille põhimõte on kirjeldatud eespool. Organismi reaktsioon sellele koormusele määrab, kas tegemist on tõesti suhkurtõvega või ainult glükoositaluvuse häirega.
Diabeedi diagnoosimiseks on vaja määrata veresuhkru tase: kui veresuhkru tase tühja kõhuga (viimase söögikorra aeg > 8 tundi) on üle 7,0 mmol/l. kaks korda erinevatel päevadel, ei tekita suhkurtõve diagnoos kahtlust.
Kui tühja kõhu veresuhkru tase on alla 7,0 mmol/l, kuid üle 5,6 mmol/l, on süsivesikute ainevahetuse olukorra selgitamiseks vajalik glükoositaluvuse test. Selle testi läbiviimise protseduur on järgmine: pärast veresuhkru sisalduse määramist tühja kõhuga (vähemalt 10 tundi tühja kõhuga) peate võtma 75 g. glükoos. Järgmine veresuhkru taseme mõõtmine tehakse 2 tunni pärast. Kui veresuhkru tase on üle 11,1, võib rääkida diabeedi olemasolust. Kui veresuhkru tase on alla 11,1 mmol / l, kuid üle 7,8 mmol / l, siis nad ütlevad, et see on süsivesikute taluvuse rikkumine. Madalama veresuhkru taseme korral tuleks analüüsi korrata 3-6 kuu pärast.
Inimese veresuhkru norm (SC norm)
Diabeedita inimestel on veresuhkru tase 3,3-5,5 mmol/l Pärast söömist võib diabeedita inimese veresuhkru tase tõusta kuni 7,8 mmol/l.
Diabeedi põhjused
Diabeedi sümptomid
 Mõlemad diabeedivormid on sümptomite poolest sarnased, kuid erinevad kulgemise olemuse poolest.
Mõlemad diabeedivormid on sümptomite poolest sarnased, kuid erinevad kulgemise olemuse poolest.
Diabeedi sümptomid:

Kui leiate selliseid sümptomeid, peate viivitamatult konsulteerima arstiga. Diabeet on väga tõsine ja ohtlik haigus.
Konsulteerige meie spetsialistiga. See on tasuta!
Peaaegu veerand diabeetikutest ei ole isegi teadlikud haiguse olemasolust. Nad elavad tavaline elu, ignoreerides keha murettekitavaid signaale, avaldab haigus jätkuvalt kahjulikku mõju siseorganitele.
Kui te ei pööra tähelepanu suhkurtõve ilmingule ega võta raviks vajalikke meetmeid, võib pikaajaline haigus põhjustada südameinfarkti, neerupuudulikkust, kahjustusi. visuaalsed funktsioonid ja muud tõsiseid probleeme tervisega.
Mõnel juhul võib diabeetik sattuda koomasse vere glükoosisisalduse suurenemise tõttu.
Haiguse tuvastamiseks peate võtma ühendust endokrinoloogiga. Kui suhkurtõve sündroomid avalduvad lastel või noortel, diagnoosib arst enamasti I tüüpi suhkurtõve.
Selle ravi seisneb insuliini igapäevases manustamises organismi.
Kui haigus avastatakse üle 40-aastastel inimestel või patsient on ülekaaluline, diagnoositakse II tüüpi diabeet.
I tüüpi diabeedi sümptomid
I tüüpi diabeet avaldub tavaliselt väga kiiresti ja kiiresti, haigus areneb välja vaid mõne päevaga.
Veresuhkru järsu tõusuga võib patsient ootamatult teadvuse kaotada ja langeda diabeetilisse koomasse. Pärast haiglas läbivaatust määrab arst suhkruhaiguse.
I tüüpi diabeedi peamised sümptomid on järgmised:
- Patsient on väga janune, ta peseb, et juua kuni viis liitrit vedelikku päevas.
- Suust on tunda atsetooni lõhna.
- Patsient tunneb pidevalt nälga ja suurenenud söögiisu, sööb palju, kuid sellest hoolimata kaotab ta järsult kaalu.
- Esineb sagedane ja tugev urineerimine, eriti öösel.
- Patsient võib nahal leida arvukalt haavu, mis paranevad väga halvasti.
- Sageli võib nahk sügelema, nahale tekivad seenhaigused või keeb.
Kaasa arvatud 1. tüüpi suhkurtõbi võib avalduda kuu aega pärast raske viirushaiguse põdemist punetiste, gripi, leetrite või muu haiguse näol.
Samuti algab haigus sageli siis, kui patsient on kogenud tõsist stressi.
II tüüpi diabeedi sümptomid
Seda tüüpi haigus ei ilmne kohe, vaid areneb järk-järgult mitme aasta jooksul. Kõige sagedamini avastatakse II tüüpi diabeet vanematel inimestel, samas kui patsient võib haigusest teada saada juhuslikult.
Patsient võib sageli tunda väsimust, halveneb ka nägemissüsteemi töö, naha haavad paranevad halvasti ja mälu väheneb.
2. tüüpi diabeedi sümptomid on järgmised:
- Patsiendi nägemine halveneb, mälu halveneb, ta väsib sageli ja kiiresti.
- Nahal leidub igasuguseid haavu, mis väljenduvad sügeluse või seeninfektsioonina ega parane hästi.
- Patsient on sageli janu ja võib juua kuni viis liitrit vedelikku päevas.
- Öösel on sagedane ja rikkalik urineerimine.
- Haavandeid võib leida sääre- ja jalalaba piirkonnas, jalad lähevad sageli tuimaks ja surisevad, liigutamine on valus.
- Naistel võib tekkida soor, millest on raske vabaneda.
- Kui haigus kulgeb, hakkab patsient kiiresti kaalust alla võtma.
- Rasketel juhtudel võib patsient kaotada nägemise, areneb.
- Ootamatu südameinfarkt või insult võib samuti põhjustada haiguse arengut.
II tüüpi diabeet on salakaval selle poolest, et pooltel inimestel võib see olla ilma sümptomiteta. Kui leiate esimesed haigusnähud, peate viivitamatult konsulteerima arstiga, ilma visiidi viivitamata.
Kell ülekaaluline, sagedane väsimus, haavade halb paranemine nahal, nägemise ja mälu halvenemine, peate muretsema ja laskma end veresuhkru taseme testida. See kõrvaldab või tuvastab haiguse varases staadiumis.
Suhkurtõbi lastel
 Sageli aetakse lapse esimesi diabeedi tunnuseid ekslikult teiste haigustega, mistõttu haigus avastatakse harva õigel ajal.
Sageli aetakse lapse esimesi diabeedi tunnuseid ekslikult teiste haigustega, mistõttu haigus avastatakse harva õigel ajal.
Enamasti alustatakse ravi siis, kui arstid tuvastavad kõrge veresuhkru taseme ja tekivad tüüpilised ägedad diabeedi sümptomid, sealhulgas diabeetiline kooma.
I tüüpi diabeeti diagnoositakse reeglina lastel ja noorukitel. Samal ajal on tänapäeval juhtumeid, kui lapsel on II tüüpi suhkurtõbi, tavaliselt võib sellist haigust leida üle 10-aastastel suure kehakaaluga lastel.
Kui lastel ilmnevad järgmised nähud, tuleb olla valvas ja konsulteerida arstiga:
- Laps on väga janune ja küsib pidevalt vett.
- Öösel võib uriinipidamatust tuvastada, isegi kui seda varem ei täheldatud.
- Laps kaotab järsult ja kiiresti kaalu.
- Võib esineda sagedast oksendamist.
- Laps on ärrituv, koolikavas ei lähe hästi.
- Nahale ilmuvad pidevalt igasugused nakkushaigused keemise, odra kujul.
- Tüdrukutel esineb puberteedieas sageli soor.
Väga sageli avastatakse haigus mõne aja pärast, kui lapsel hakkavad ilmnema ägedad sümptomid. Kahjuks ei ole harvad juhused, kus arstid alustavad ravi, kui suust on tunda atsetoonilõhna, keha on dehüdreeritud või laps langeb diabeetilisse koomasse.
Seega on haiguse ägedad sümptomid:
- Pidev oksendamine.
- Keha on tugevalt dehüdreeritud. Sellest hoolimata kogeb laps sagedast tung urineerida.
- Dehüdratsiooni tõttu muutub laps väga kõhnaks, keha kaotab rasvarakke ja lihasmassi.
- Laps hingab ebatavaliselt – ühtlaselt, harva, sügavalt mürarikkalt sisse ja jõuliselt välja hingates.
- Suust on püsiv atsetooni lõhn.
- Laps võib kaotada teadvuse, olla loid, desorienteeritud ruumis.
- Sest šokiseisund võib esineda kiire pulss ja sinised jäsemed.
Imikute diabeeti diagnoositakse väga harva, kuid selle haiguse juhtumeid on registreeritud. Fakt on see, et imikutel ei ole võimalust rääkida, mistõttu nad ei saa teada anda, et neil on janu või halb enesetunne.
Kuna vanemad kasutavad tavaliselt mähkmeid, on väga raske tuvastada, et laps urineerib palju rohkem kui tavaliselt.
Vahepeal saab eristada imikutel esineva haiguse peamisi tunnuseid:
- Hoolimata asjaolust, et laps sööb sageli palju, ei võta ta kaalus juurde, vaid vastupidi, kaotab kiiresti.
- Beebi võib sageli ilmutada ärevust, rahuneb alles pärast jooki.
- Suguelunditel võib sageli leida mähkmelöövet, mida ei saa ravida.
- Pärast uriini kuivamist muutub mähe justkui tärgeldatud.
- Kui uriin satub põrandale, jäävad kleepuvad laigud.
Imikute haiguse ägedad sümptomid on sagedane oksendamine, tugev dehüdratsioon ja mürgistus.
Diabeedi ilming koolilastel
Noorematel õpilastel täheldatakse tavaliselt kõiki eelnevalt loetletud tavalisi ja ägedaid sümptomeid. Kuna suhkurtõbi maskeerub sageli teiste haigustena, võib seda olla raske õigeaegselt ära tunda.
Nendel lastel kulgeb haigus raskes ja ebastabiilses vormis.
Pole harvad juhud, kui arst diagnoosib diabeedi ajal hüpoglükeemia. Selle nähtuse tunnuste hulka kuuluvad järgmised sümptomid:
- Lapsel on pidev ärevus, ta on sageli kontrollimatu.
- Kaasa arvatud õpilane, vastupidi, võib kogeda pidevat letargiat, uinuda klassis või muul ebatavalisel ajal.
- Laps keeldub pidevalt söömast. Kui proovite süüa maiustusi, täheldatakse oksendamist.
Oluline on mõista, et lapsele tasub maiustusi anda ainult tõelise hüpoglükeemia korral. Kui kahtlustate haigust, peate mõõtma veresuhkru taset ja pöörduma viivitamatult arsti poole. Kui hüpoglükeemia muutub raskeks, võib see põhjustada ajukahjustusi ja puude.
Noorukitel ja täiskasvanutel on peaaegu samad diabeedi tunnused. Samal ajal on oluline arvestada mõne vanusega seotud eripäraga.
Noorukieas areneb haigus erinevalt koolieelikutele ja noorematele koolilastele sujuvalt. Haiguse esialgne staadium võib kesta mitu kuud. Sageli peetakse selles vanuses patsientide diabeedi peamisi tunnuseid ekslikult neuroosiks või aeglaseks infektsiooniks.
Peate olema valvas, kui teismeline kaebab, et:
- Väsib kiiresti;
- Tunneb end sageli nõrgana;
- Tal on sageli peavalu;
- Ta on ärrituv;
- Lapsel ei lähe koolis hästi.
Kuudel enne ägedate haigusnähtude ilmnemist võivad lapsel esineda perioodilised hüpoglükeemiahood. Samal ajal ei kaota teismeline teadvust ega koge krampe, vaid kogeb tugevat magusavajadust.
Sarnane nähtus võib olla haiguse esialgse staadiumi ilming immuunsüsteemi rünnaku ajal kõhunäärme beetarakkudele.
Enne haiguse avaldumist võib teismeline pidevalt kannatada nahahaigused. Ketoatsidoosi korral võib patsiendil tekkida tugev kõhuvalu ja oksendamine. Neid sümptomeid peetakse sageli ekslikult soolemürgituseks või äge apenditsiit, sel põhjusel otsivad vanemad abi kõigepealt kirurgilt.
Eriti ägedad haigusnähud võivad ilmneda puberteedieas. See on tingitud asjaolust, et hormonaalsete muutuste tõttu väheneb kudede tundlikkus insuliini suhtes. Samuti otsustavad vanemad õpilased sageli dieedi kasuks, keelduvad kehalisest treeningust ja unustavad vajaduse regulaarselt kehasse insuliini süstida.
II tüüpi diabeedi tunnused lastel
Tänapäeval on haigus muutunud märgatavalt nooremaks, nii et 2. tüüpi diabeeti avastatakse nüüd isegi lastel. Seda haigust leitakse üle 10-aastastel rasvunud lastel.
Riskirühma kuuluvad peamiselt metaboolse sündroomiga lapsed. Need märgid hõlmavad järgmist:
- Rasvumine kõhupiirkonnas;
- arteriaalne hüpertensioon;
- Suurenenud triglütseriidide ja kolesterooli tase veres;
- Rasvane maks.
Seda tüüpi diabeet võib alata puberteedieas, mis esineb poistel 12-18-aastaselt ja tüdrukutel 10-17-aastaselt. Tavaliselt avaldub haigus siis, kui sugulaste seas on juba diabeedijuhtumeid.
Vaid viiendik noortest patsientidest kurdab janutunnet, sagedast urineerimist ja kehakaalu järsku langust. Teistel teismelistel on haiguse tavalised sümptomid:
- Raskete krooniliste infektsioonide esinemine;
- Kehakaalu suurenemine;
- Raskused urineerimisel;
- Uriinipidamatus.
Reeglina avastatakse haigus siis, kui noored läbivad rutiinse arstliku läbivaatuse terapeudi juures. Arstid pööravad vere ja uriini analüüsimisel tähelepanu kõrgele suhkrusisaldusele.
Erinevus 1. ja 2. tüüpi diabeedi vahel
I tüüpi diabeet tekib tavaliselt ootamatult pärast seda, kui see muutub ägedaks. Patsiendil võib tekkida diabeetiline kooma või raske atsidoos. Sel juhul ei muutu rasvumine reeglina haiguse põhjuseks.
Samuti võib haigus end tunda anda pärast seda, kui patsiendil on olnud nakkushaigus. Diabeetik võib tunda söögiisu suurenemist, janutunnet, suukuivust. Suurenenud vajadus sagedase urineerimise järele öösel. Sellisel juhul võib patsient tugevalt ja kiiresti kaalust alla võtta, kogeda nõrkust, sügelust.
Sageli ei suuda organism nakkushaigustega toime tulla, mille tagajärjel haigus kestab kaua. Esimesel nädalal võib patsient tunda, et tema nägemine on halvenenud. Kui sel ajal diabeeti õigel ajal ei avastata ja ravi ei alustata, võib kehas insuliinipuuduse tõttu tekkida diabeetiline kooma.
Teist tüüpi diabeet hõlmab haiguse järkjärgulist arengut. Kui varem arvati, et haigestuvad ainult eakad, siis tänapäeval hakkab see piir tasapisi hägustuma. Sealhulgas sarnast haigust diagnoositakse suurenenud kehakaaluga inimestel.
Patsient ei pruugi tervise halvenemist märgata mitu aastat. Kui sel perioodil ravi ei toimu, võivad tekkida tüsistused kardiovaskulaarsüsteemi valdkonnas. Diabeetikud tunnevad nõrkust ja mälu halvenemist, väsivad kiiresti.
Sageli on sellised nähud seotud keha vanuseomadustega ja 2. tüüpi diabeet avastatakse ootamatult. Haiguse õigeaegseks diagnoosimiseks on vaja regulaarselt läbida arstlik läbivaatus.
Reeglina avastatakse diabeet inimestel, kellel on sarnase diagnoosiga sugulased. Samuti võib haigus ilmneda perekondliku kalduvusega rasvumisele.
Eelkõige kuuluvad riskirühma naised, kelle laps kaalub üle 4 kilogrammi, samas kui raseduse ajal oli veresuhkru tõus.
Peamised sümptomid ja nende põhjused
Et mõista, miks teatud haiguse tunnused ilmnevad, tasub diabeedi sümptomeid üksikasjalikumalt kaaluda.
Suurenenud janu ja sagedane soov urineerida ilmnevad veresuhkru taseme olulise tõusu tõttu. Keha üritab liigset glükoosi uriiniga väljutada. Suure kontsentratsiooni tõttu võib aga märkimisväärne osa glükoosist jääda neerudesse. Sellest vabanemiseks on vaja suures koguses uriini - sellest ka suurenenud vedelikuvajadus. Kui patsient käib sageli öösel tualetis ja joob palju, tuleb sellele erilist tähelepanu pöörata.
Diabeedi korral on sageli suust püsiv atsetooni lõhn. Ägeda insuliinipuuduse või selle ebaefektiivse toime tõttu hakkavad rakud rasvavarude abil täienema. Rasvade lagunemisel tekivad ketokehad, koos kõrge kontsentratsioon mis tekitavad suus atsetoonilõhna.
Lõhn on tugevalt tunda, kui patsient hingab. Selle välimus viitab esiteks sellele, et keha on ümber korraldatud rasvadest toituma. Kui vajalikke meetmeid ei võeta õigeaegselt ega manustata vajalikku insuliini annust, võib ketokehade kontsentratsioon oluliselt suureneda.
See omakorda viib selleni, et kehal pole aega end kaitsta ja vere happesus muutub. Kui vere pH ületab 7,35-7,45, võib patsient tunda loidust ja uimasust, isu väheneb, iiveldus ja kerge kõhuvalu. Arstid diagnoosivad diabeetilise ketoatsidoosi.
Ei ole harvad juhud, kui inimene langeb mingil põhjusel koomasse. Selline tüsistus on väga ohtlik, võib põhjustada patsiendi puude või isegi surma.
Siiski on oluline teada, et hingeõhust tekkivat atsetoonilõhna on tunda ka siis, kui II tüüpi diabeeti põdevat patsienti ravitakse süsivesikutevaese dieediga. Veres ja kudedes ketokehade arv suureneb, vahepeal ei ole näitajad madalamad kui vere happesuse norm 7,30. Sel põhjusel, vaatamata atsetooni lõhnale, ei avalda ketokehad kehale toksilist mõju.
Diabeetik omakorda kaotab kaalu ja vabaneb liigsest keharasvast.
Söögiisu suureneb diabeedihaigetel oluliselt, kui keha kogeb insuliinipuudust. Vaatamata suhkru rohkusele veres ei omasta rakud seda insuliinipuuduse või hormooni kehale vale mõju tõttu. Seetõttu hakkavad rakud nälgima ja saadavad ajule signaali, mille tagajärjel suureneb inimese isu.
Hoolimata piisavast toitumisest ei suuda kuded sissetulevaid süsivesikuid täielikult omastada, mistõttu võib isu jätkuda seni, kuni insuliinipuudus kaob.
Diabeetikul tekib sageli nahasügelus, ta põeb seeninfektsioone ja naistel tekib soor. See on tingitud asjaolust, et liigne suhkur eritub higiga. Seennakkused seevastu levivad soojas keskkonnas, samas kui suhkru suurenenud kontsentratsioon on nende toitumise põhikeskkond. Kui viite oma veresuhkru taseme tagasi normaalseks, kaovad reeglina nahahaigustega seotud probleemid.
Diabeetikutel on nahapinnal tekkinud haavad väga raskesti paranevad. Selle põhjuseks on ka suurenenud glükoosisisaldus veres. Suhkru suur kontsentratsioon avaldab toksilist mõju veresoonte seintele ja pestud rakkudele.
See aeglustab haava paranemise protsessi. See loob soodsa keskkonna bakterite ja seente arenguks.
Seetõttu vananeb suhkurtõvega naiste nahk varakult ja muutub lõtvaks.
Haiguse kinnitus
Diabeedi raskete sümptomite esinemisel piisab kõrge veresuhkru tuvastamiseks ja vajalike ravimeetmete võtmiseks vereanalüüsist. Vahepeal, kui analüüs näitas glükoosi ülehinnatud kontsentratsiooni ja haiguse sümptomeid pole, võib diabeedi diagnoosimine olla keeruline.
Nagu teate, võib raske stressi tõttu veresuhkru tase tõusta. äge infektsioon, füüsiline vigastus. Sel põhjusel on näitajad ajutised ja taastuvad sageli pärast seda vajalik ravi. Sellega seoses ei diagnoosi arstid sümptomite puudumisel diabeeti, isegi kui analüüs näitas veresuhkru tõusu.
Suhkurtõbi on endokriinsüsteemi haiguste rühm, mis areneb insuliini (hormooni) puudumise või puudumise tõttu organismis, mille tulemuseks on glükoosi (suhkru) taseme oluline tõus veres (hüperglükeemia). Avaldub janutundes, eritunud uriini hulga suurenemises, suurenenud söögiisu, nõrkus, pearinglus, haavade aeglane paranemine jne. Haigus on krooniline, sageli progresseeruva kuluga.
Õigeaegne diagnoos annab patsiendile võimaluse raskete tüsistuste tekkimist edasi lükata. Kuid alati ei ole võimalik esimesi diabeedi tunnuseid ära tunda. Selle põhjuseks on inimeste elementaarsete teadmiste puudumine selle haiguse ja madal tase arstiabi otsivad patsiendid.
Mis on suhkurtõbi?
Suhkurtõbi on endokriinsüsteemi haigus, mis on põhjustatud kõhunäärmehormooni insuliini absoluutsest või suhtelisest puudusest organismis, mille tagajärjeks on hüperglükeemia (vere glükoosisisalduse püsiv tõus).
Sõna "diabeet" tähendus koos kreeka keel- "aegumine". Seetõttu tähendab mõiste "suhkurtõbi" "suhkru kaotamist". Sel juhul kuvatakse haiguse peamine sümptom - suhkru eritumine uriiniga.
Umbes 10% maailma elanikkonnast kannatab diabeedi all, kuid antud varjatud vormid haiguste korral võib see näitaja olla 3-4 korda suurem. See areneb kroonilise insuliinipuuduse tagajärjel ning sellega kaasnevad süsivesikute, valkude ja rasvade ainevahetuse häired.
Vähemalt 25% diabeediga inimestest ei ole oma haigusest teadlikud. Nad ajavad rahulikult oma asju, ei pööra tähelepanu sümptomitele ja sel ajal hävitab diabeet järk-järgult nende keha.
Kõrge veresuhkru tase võib põhjustada peaaegu kõigi organite talitlushäireid kuni surmani. Mida kõrgem on veresuhkru tase, seda ilmsem on selle toime tulemus, mis väljendub:
- ülekaalulisus
- rakkude glükosüülimine (sahharifitseerimine);
- keha mürgistus koos närvisüsteemi kahjustusega;
- veresoonte kahjustus;
- sekundaarsete haiguste areng, mis mõjutavad aju, südant, maksa, kopse, elundeid
- Seedetrakt, lihased, nahk, silmad;
- minestamise ilmingud, kooma;
- surmav tulemus.
Põhjused

Diabeedil on palju põhjuseid, mis põhinevad organismi endokriinsüsteemi talitluse üldisel häirel, mis põhinevad kas kõhunäärme toodetava hormooni insuliini puudusel või maksa töövõimetusel. ja kehakuded, et glükoosi korralikult töödelda ja omastada.
Selle hormooni puudumise tõttu organismis suureneb glükoosi kontsentratsioon veres pidevalt, mis põhjustab ainevahetushäireid, kuna insuliin täidab olulist funktsiooni glükoosi töötlemise kontrollimisel kõigis keharakkudes ja kudedes.
Üks põhjusi on pärilik eelsoodumus. Kui inimese peres on diabeetikuid, siis on tal teatav risk haigestuda sellesse haigusse, eriti kui ta juhib ebatervislikku eluviisi. Diabeedi arengu põhjused, isegi neil, kellel pole eelsoodumust, võivad olla:
- alatoitumine ja maiustuste kuritarvitamine;
- stress ja mitmesugused psühho-emotsionaalne stress; põdes rasket haigust;
- maksa häired; elustiili muutus;
- ülekaal;
- raske töö jne.
Paljud inimesed arvavad, et diabeet tekib magusaisu puhul. See on suures osas müüt, kuid omajagu tõde on ka selles, kas või juba seetõttu, et liigne tarbimine toob magusalt kaasa ülekaalu ja hiljem rasvumise, mis võib olla tõukejõuks 2. tüüpi diabeedi tekkeks.
Arengut soodustavad riskitegurid seda haigust lastel on neil mõnes mõttes sarnasusi ülaltoodud teguritega, kuid ka siin on omapära. Toome välja peamised tegurid:
- lapse sünd suhkurtõvega vanematele (kui ühel või mõlemal on see haigus);
- sagedane viirushaiguste esinemine lapsel;
- teatud ainevahetushäirete (rasvumine jne) esinemine;
- sünnikaal 4,5 kg või rohkem;
- vähenenud immuunsus.
Tähtis: mida vanemaks inimene saab, seda suurem on kõnealuse haiguse tõenäosus. Statistika kohaselt kahekordistub diabeedi tekkimise tõenäosus iga 10 aasta järel.
Tüübid
Kuna suhkurtõvel on palju erinevaid etioloogiaid, tunnuseid, tüsistusi ja loomulikult ka ravitüüpi, on eksperdid loonud selle haiguse klassifitseerimiseks üsna mahuka valemi. Mõelge diabeedi tüüpidele, tüüpidele ja astmetele.
1. tüüpi diabeet
I tüüpi diabeet, mis on seotud hormooninsuliini absoluutse puudusega, ilmneb tavaliselt ägedalt, järsult, muutub kiiresti ketoatsidoosi seisundiks, mis võib viia ketoatsidootilise koomani. Kõige sagedamini avaldub see noortel inimestel: reeglina on enamik neist patsientidest alla kolmekümne aasta vanad. Ligikaudu 10-15% diabeedihaigete koguarvust põeb seda haigusvormi.
I tüüpi diabeedist on peaaegu võimatu täielikult taastuda, kuigi esineb pankrease funktsioonide taastamise juhtumeid, kuid see on võimalik ainult eritingimustel ja looduslikul toortoidul.
Keha säilitamiseks on vaja insuliini süstida kehasse süstlaga. Kuna insuliin hävib seedetrakti, siis on insuliini võtmine tablettide kujul võimatu. Insuliini manustatakse koos toiduga.
2. tüüpi diabeet
Teine tüüp, mida varem nimetati insuliinist sõltumatuks, kuid see määratlus pole täpne, kuna selle tüübi progresseerumisel võib osutuda vajalikuks insuliini asendusravi. Seda tüüpi haiguste korral jääb insuliini tase esialgu normaalseks või isegi normaalsest kõrgemaks.
Kuid keharakud, eelkõige adipotsüüdid (rasvarakud), muutuvad selle suhtes tundetuks, mis põhjustab vere glükoosisisalduse tõusu.
kraadid
See eristamine aitab kiiresti mõista, mis juhtub patsiendiga haiguse erinevatel etappidel:
- 1 kraad (mahe). I astme suhkurtõbi on algstaadiumis, see tähendab, et glükoosisisaldus ei ületa 6,0 mol / l. Patsiendil ei esine suhkurtõve tüsistusi, seda kompenseeritakse dieedi ja spetsiaalsete ravimite abil.
- 2. aste (keskmine). 2. tüüpi diabeet on ohtlikum ja raskem, kuna glükoosisisaldus hakkab ületama normaalset kogust. Samuti on häiritud elundite, täpsemalt: neerude, silmade, südame, vere ja närvikudede normaalne talitlus. Samuti jõuab veresuhkru tase üle 7,0 mol/l.
- 3 kraadi (raske). Haigus on ägedamas staadiumis, mistõttu on seda ravimite ja insuliini abil raske ravida. Suhkur ja glükoos ületavad 10-14 mol/l, mis tähendab, et vereringe töö halveneb ja vererõngad võivad kokku kukkuda, põhjustades vere- ja südamehaigusi.
- 4 kraadi. Suhkurtõve kõige raskemat kulgu iseloomustab kõrge glükoosisisaldus - kuni 25 mmol / l, nii glükoos kui ka valk erituvad uriiniga, seisundit ei paranda ükski ravim. Selle vaadeldava haiguse astmega diagnoositakse sageli neerupuudulikkus, gangreen. alajäsemed, diabeetilised haavandid.
Esimesed diabeedi tunnused

Esimesed diabeedi tunnused on tavaliselt seotud suurenenud tase veresuhkur. Tavaliselt ei ületa see näitaja tühja kõhuga kapillaarveres 5,5 mM/l ja päeva jooksul - 7,8 mM/l. Kui keskmine päevane suhkrusisaldus tõuseb üle 9-13 mM/l, võivad patsiendil tekkida esimesed kaebused.
Mõnede märkide järgi on suhkurtõbe kerge ära tunda varases staadiumis. Kerge muutus seisundis, mida igaüks võib märgata, viitab sageli selle haiguse esimese või teise tüübi arengule.
Märgid, millele tähelepanu pöörata:
- Liigne ja sagedane urineerimine (umbes iga tund)
- Naha ja suguelundite sügelus.
- Tugev janu või suurenenud vajadus juua palju vedelikku.
- Kuiv suu.
- Halb haavade paranemine.
- Esiteks palju kaalu, millele järgneb selle vähenemine toidu, eriti süsivesikute imendumise rikkumise tõttu.
Diabeedi nähtude avastamisel välistab arst muud sarnaste kaebustega haigused (suhkru insipidus, nefrogeenne, hüperparatüreoidism ja teised). Järgmisena viiakse läbi uuring, et selgitada välja diabeedi põhjus ja tüüp. Mõnel tüüpilisel juhul pole see ülesanne keeruline ja mõnikord on vaja täiendavat uurimist.
Diabeedi sümptomid
Sümptomite raskusaste sõltub täielikult järgmistest parameetritest: insuliini sekretsiooni vähenemise tase, haiguse kestus, patsiendi keha individuaalsed omadused.
Mõlemale diabeeditüübile on iseloomulik sümptomite kompleks. Sümptomite raskusaste sõltub insuliini sekretsiooni vähenemise astmest, haiguse kestusest ja patsiendi individuaalsetest omadustest:
- Pidev janu ja sagedane urineerimine. Mida rohkem patsient joob, seda rohkem ta tahab;
- Suurenenud söögiisu korral kaob kaal kiiresti;
- Silmade ette ilmub “valge loor”, kuna silma võrkkesta verevarustus on häiritud;
- Seksuaalaktiivsuse häired ja potentsi langus on suhkurtõve esinemise sagedased tunnused;
- Immuunsüsteemi funktsioonide vähenemise tõttu tekivad patsientidel sagedased külmetushaigused (ARVI, ägedad hingamisteede infektsioonid). Selle taustal on haavade aeglane paranemine, pearinglus ja raskustunne jalgades;
- Säärelihaste pidevad krambid on lihassüsteemi töö käigus tekkinud energiapuuduse tagajärg.
| 1. tüüpi diabeet | Patsiendid võivad 1. tüüpi diabeedi korral kaevata järgmiste sümptomite üle:
|
| 2. tüüpi diabeet | 2. tüüpi diabeeti iseloomustavad: tavalised kaebused:
|
Kuidas diabeet naistel avaldub?
- Järsk kaalulangus- märk, mis peaks olema murettekitav, kui dieeti ei järgita, säilib varasem isu. Kaalulangus tekib insuliini puuduse tõttu, mis on vajalik glükoosi viimiseks rasvarakkudesse.
- Janu. Diabeetiline ketoatsidoos põhjustab kontrollimatut janu. Sellisel juhul jääb suukuivus isegi siis, kui joote suures koguses vedelikku.
- Väsimus . Füüsilise kurnatuse tunne, millel mõnel juhul pole ilmset põhjust.
- suurenenud söögiisu(polüfaagia). Eriline käitumine, mille puhul keha küllastumist ei toimu isegi pärast võtmist piisav toit. Polüfaagia on suhkurtõve glükoosi metabolismi häire peamine sümptom.
- Ainevahetusprotsesside rikkumine naise kehas põhjustab keha mikrofloora rikkumist. Ainevahetushäirete arengu esimesteks tunnusteks on tupepõletikud, mida praktiliselt ei ravita.
- Mitteparanevad haavad, muutudes haavanditeks – tüdrukute ja naiste iseloomulikud esimesed diabeedi tunnused
- Osteoporoos - kaasneb insuliinsõltuva suhkurtõvega, kuna selle hormooni puudumine mõjutab otseselt luukoe moodustumist.
Diabeedi tunnused meestel
Peamised märgid, mis näitavad, et diabeet meestel areneb, on järgmised:
- üldise nõrkuse ilmnemine ja töövõime märkimisväärne langus;
- naha sügeluse ilmnemine, eriti see kehtib suguelundite piirkonna naha kohta;
- seksuaalhäired, põletikuliste protsesside progresseerumine ja impotentsuse areng;
- janutunne, kuivus suuõõne ja pidev näljatunne;
- haavandiliste moodustiste ilmumine nahale, mis kaua aegaära parane;
- sagedane tung urineerida;
- hammaste lagunemine ja juuste väljalangemine.
Tüsistused
Iseenesest ei kujuta diabeet inimese elule ohtu. Selle tüsistused ja nende tagajärjed on ohtlikud. On võimatu mainimata jätta mõnda neist, mida sageli kohtab või mis kujutavad otsest ohtu patsiendi elule.
Esiteks tuleb seda kõige rohkem märkida teravad vormid tüsistused. Iga diabeetiku elu jaoks kujutavad sellised tüsistused suurimat ohtu, sest need võivad lõppeda surmaga.
Ägedate tüsistuste hulka kuuluvad:
- ketoatsidoos;
- hüperosmolaarne kooma;
- hüpoglükeemia;
- piimhappe kooma.
Diabeedi ägedad tüsistused on identsed nii lastel kui ka täiskasvanutel
Kroonilised tüsistused hõlmavad järgmist:
- entsefalopaatia diabeetilises vormis;
- nahakahjustused folliikulite kujul ja struktuursed muutused otse epidermises;
- diabeetilise jala või käe sündroom;
- nefropaatia;
- retinopaatia.
Tüsistuste ennetamine
Ennetavad meetmed hõlmavad järgmist:
- kaalujälgimine - kui patsient tunneb, et ta võtab juurde liigseid kilosid, peate võtma ühendust toitumisspetsialistiga ja saama nõu ratsionaalse menüü koostamiseks;
- pidev füüsiline aktiivsus - raviarst ütleb teile, kui intensiivsed need peaksid olema;
- pidev vererõhu jälgimine.
Tüsistuste ennetamine suhkurtõve korral on see võimalik püsiv ravi ja vere glükoositaseme hoolikas jälgimine.
Diagnostika
Suhkurtõbi avaldub inimesel järk-järgult, seetõttu eristavad arstid selle arengu kolme perioodi.
- Inimestel, kellel on teatud riskitegurite olemasolu tõttu kalduvus haigusele, avaldub nn diabeedieelne periood.
- Kui glükoos on juba häiretega assimileerunud, kuid haiguse tunnused veel ei ilmne, diagnoositakse patsiendil varjatud suhkurtõve periood.
- Kolmas periood on haiguse enda areng.
Diabeedi kahtluse korral tuleb see diagnoos kas kinnitada või ümber lükata. Selleks on mitmeid laboreid ja instrumentaalsed meetodid. Need sisaldavad:
- Vere glükoosisisalduse määramine. Normaalväärtus- 3,3-5,5 mmol / l.
- Glükoosi tase uriinis. Tavaliselt suhkrut uriinis ei tuvastata.
- Vereanalüüs glükosüülitud hemoglobiini määramiseks. Norm on 4–6%.
- IRI (immunoreaktiivne insuliin). Normaalväärtus on 86-180 nmol / l. I tüüpi diabeedi korral on see vähenenud, 2. tüüpi diabeedi korral on see normaalne või kõrgem.
- Uriinianalüüs - neerukahjustuse diagnoosimiseks.
- Naha kapillaroskoopia, Doppleri ultraheli - veresoonte kahjustuse diagnoosimiseks.
- Silmapõhja uurimine - võrkkesta kahjustuste diagnoosimiseks.
Veresuhkur
Milliseid suhkrusisaldusi peetakse normaalseks?
- 3,3–5,5 mmol / l on veresuhkru norm, olenemata teie vanusest.
- 5,5 - 6 mmol / l on prediabeet, glükoositaluvuse häire.
- 6. 5 mmol/l ja üle selle on juba diabeet.
Diabeedi diagnoosi kinnitamiseks on vajalik korduv veresuhkru mõõtmine erinevatel kellaaegadel. Mõõtmisi on kõige parem teha meditsiinilaboris ja enesekontrolliseadmeid ei tasu usaldada, kuna neil on märkimisväärne mõõtmisviga.
Märge: valepositiivsete tulemuste välistamiseks on vaja mitte ainult mõõta veresuhkru taset, vaid teha ka glükoositaluvuse test (suhkrukoormusega vereproov).
Normid on toodud tabelis (mõõteväärtus - mmol / l):
| Tulemuste hindamine | kapillaarveri | hapnikuvaba veri |
|
||
| Tühja kõhu veresuhkru test |
|
|
| Pärast glükoosi võtmist (2 tunni pärast) või pärast söömist |
|
|
|
||
| tühja kõhuga |
|
|
| Pärast glükoosi või pärast sööki |
|
|
| tühja kõhuga |
|
|
| Pärast glükoosi või pärast sööki |
|
|
Kõik diabeediga patsiendid peaksid konsulteerima selliste spetsialistidega:
- Endokrinoloog;
- kardioloog;
- neuropatoloog;
- Oftalmoloog;
- Kirurg (veresoonkonna või eriarst - lastearst);
Kuidas ravida diabeeti täiskasvanutel?

Arstid määravad suhkurtõve kompleksravi, et säilitada normaalne veresuhkru tase. Sel juhul on oluline arvestada, et ei tohiks lubada hüperglükeemiat, see tähendab suhkru taseme tõusu ega hüpoglükeemiat, st selle langust.
Enne ravi alustamist on vaja läbi viia keha täpne diagnoos, sest. sellest sõltub positiivne taastumise prognoos.
Diabeedi ravi eesmärk on:
- veresuhkru taseme alandamine;
- ainevahetuse normaliseerimine;
- diabeedi tüsistuste ennetamine.
Ravi insuliinipreparaatidega
Diabeedi raviks kasutatavad insuliinipreparaadid jagunevad toime kestuse järgi 4 kategooriasse:
- Ultralühiajaline toime (toime algus - 15 minuti pärast, toime kestus - 3-4 tundi): insuliin LizPro, insuliin aspart.
- Kiire toime (toime algab 30 minuti–1 tunni pärast; toime kestus on 6–8 tundi).
- Keskmine toimeaeg (toime algab 1-2,5 tunni pärast, toimeaeg on 14-20 tundi).
- Pikatoimeline (toime algus - 4 tunni pärast; toime kestus kuni 28 tundi).
Insuliini režiimid on rangelt individuaalsed ja iga patsiendi jaoks valitakse diabeedi- või endokrinoloogi poolt.
Diabeedi tõhusa ravi võti on hoolikas veresuhkru taseme kontroll. Siiski on võimatu teha laboratoorseid analüüse mitu korda päevas. Appi tulevad kaasaskantavad glükomeetrid, mis on kompaktsed, neid on lihtne kaasa võtta ja kontrollida glükoosi taset seal, kus vaja.
Lihtsustab venekeelse liidese kontrollimist, märgistab enne ja pärast sööki. Seadmeid on äärmiselt lihtne kasutada, samas kui mõõtmistäpsuse poolest erinevad need. Hoidke oma diabeet kontrolli all kaasaskantava glükomeetriga
Dieet

Dieediteraapia peamised põhimõtted on järgmised:
- igapäevase kalorisisalduse rangelt individuaalne valik, kergesti seeditavate süsivesikute täielik välistamine;
- rangelt arvutatud rasvade, valkude, vitamiinide ja süsivesikute füsioloogiliste koguste sisaldus;
- osatoidud ühtlaselt jaotunud süsivesikute ja kaloritega.
Diabeedi dieedis peaks süsivesikute, rasvade ja valkude suhe olema võimalikult lähedane füsioloogilisele:
- 50-60% kogu kaloritest peaks tulema süsivesikutest
- 25-30% rasvade puhul,
- 15-20% valkude puhul.
Samuti peaks toit sisaldama vähemalt 4–4,5 grammi süsivesikuid kilogrammi kehakaalu kohta, 1–1,5 grammi valku ja 0,75–1,5 grammi rasva päevases annuses.
Dieet suhkurtõve ravis (tabel nr 9) on suunatud süsivesikute ainevahetuse normaliseerimisele ja rasvade ainevahetuse häirete ennetamisele.
Füüsiline treening
Regulaarne treening aitab alandada veresuhkru taset. Lisaks aitab kehaline aktiivsus kaalust alla võtta.
Ei ole vaja igapäevaselt sörkida ega jõusaalis käia, piisab, kui teha 3 korda nädalas vähemalt 30 minutit, et teha mõõdukat kehalist aktiivsust. Igapäevane kõndimine on väga kasulik. Isegi kui töötate mitu päeva nädalas enda nimel isiklik krunt sellel on positiivne mõju teie heaolule.
Rahvapärased abinõud
Enne diabeedi rahvapäraste meetodite kasutamist on võimalik alles pärast endokrinoloogiga konsulteerimist, sest. on vastunäidustusi.
- Sidrun ja munad. Pigista 1 sidrunist mahl välja ja sega sellega korralikult 1 toores muna. Jooge saadud preparaati 60 minutit enne sööki 3 päeva jooksul.
- Takjas mahl. Mais välja kaevatud purustatud takjajuurest saadud mahl alandab tõhusalt suhkrutaset. Seda võetakse kolm korda päevas 15 ml kohta, lahjendades seda kogust 250 ml jaheda keedetud veega.
- Suhkurtõve korral hauta küpseid kreeka pähkleid (40 g) 0,5 liitris keevas vees madalal kuumusel 1 tund; võtta 3 korda päevas, 15 ml.
- psülliumi seemned(15 g) valatakse emailitud kaussi koos klaasi veega, keedetakse madalal kuumusel 5 minutit. Jahutatud puljong filtreeritakse ja võetakse 1 magustoidulusikatäis 3 korda päevas.
- Küpsetatud sibul. Normaliseerige suhkur, eriti algfaasis haigus, võite kasutada igapäevane kasutamine küpsetatud sibul hommikul tühja kõhuga. Tulemust saab jälgida 1-1,5 kuu pärast.
- Hirss nakkuse vastu. Nakkuse vastu ja diabeedi ennetamiseks võite kasutada järgmist retsepti: võtta 1 peotäis hirssi, loputada, valada 1 liiter keeva veega, lasta üleöö ja juua päeva jooksul. Korrake protseduuri 3 päeva.
- Sireli pungad. Sireli pungade infusioon aitab normaliseerida vere glükoosisisaldust. Aprilli lõpus korjatakse pungad paisumise staadiumis, kuivatatakse, hoitakse klaaspurki või paberkotis ja kasutatakse ära. aasta läbi. Päevane infusioonimäär: 2 spl. lusikad kuiva toorainet valage 0,4 liitrit keeva veega, nõudke 5-6 tundi, filtreerige, jagage saadud vedelik 4 korda ja jooge enne sööki.
- Aitab alandada veresuhkrut ja tavalist loorberilehte. Peate võtma 8 tükki loorberilehte ja valama see 250 grammi "jaheda" keeva veega, infusiooni tuleb infundeerida termoses umbes päev. Infusioon võetakse soojalt, iga kord, kui peate infusiooni termosest välja kurnama. Võtke 1/4 tassi kakskümmend minutit enne sööki.
Diabeediga inimese elustiil
Põhireeglid, mida diabeetikutele järgida:
- toitu sööma, kiudainerikas. Need on kaer, kaunviljad, köögiviljad ja puuviljad.
- Vähendage oma kolesterooli tarbimist.
- Kasutage suhkru asemel magusainet.
- Sööge sageli, kuid väikestes kogustes. Patsiendi keha saab paremini hakkama väikese toiduannusega, kuna see vajab vähem insuliini.
- Kontrollige mitu korda päevas oma jalgu kahjustuste suhtes, peske iga päev seebiga ja kuivatage.
- Kui olete ülekaaluline, on kaalulangus esimene samm diabeedi juhtimisel.
- Nakkuse vältimiseks hoolitsege kindlasti oma hammaste eest.
- Vältige stressi.
- Andke oma vereanalüüs regulaarselt.
- Ärge ostke ravimeid ilma retseptita
Prognoos
Diagnoositud suhkurtõvega patsiendid registreeritakse endokrinoloogi juures. Õige elustiili, toitumise, ravi korraldamisega võib patsient tunda end rahuldavalt aastaid. Süvendada suhkurtõve prognoosi ja vähendada ägedate ja krooniliselt arenevate tüsistustega patsientide eeldatavat eluiga.
Ärahoidmine
Diabeedi arengu vältimiseks on vaja järgmisi ennetavaid meetmeid:
- tervislik toitumine: toitumise kontroll, dieedi pidamine – suhkru vältimine ja rasvased toidud vähendab diabeedi tekkeriski 10-15% võrra;
- füüsiline aktiivsus: normaliseerida vererõhku, immuunsust ja vähendada kehakaalu;
- suhkru taseme kontroll;
- stressi välistamine.
Kui olete ilmunud omadused diabeet, siis mine kindlasti endokrinoloogi vastuvõtule, sest. varajane ravi on kõige tõhusam. Hoolitse enda ja oma tervise eest!
7.1. DIABEEDI KLASSIFIKATSIOON
Diabeet(DM) - metaboolsete haiguste rühm, mida iseloomustab insuliini sekretsiooni ja/või insuliini toime efektiivsuse halvenemise tõttu tekkiv hüperglükeemia. Diabeedi korral tekkiva kroonilise hüperglükeemiaga kaasnevad tüsistused paljudest elunditest ja süsteemidest, eelkõige südamest, veresoontest, silmadest, neerudest ja närvidest. DM kokku mõjutab 5-6% elanikkonnast. Maailma majanduslikult arenenud riikides suureneb diabeedihaigete arv iga 10-15 aasta järel 2 korda. Oodatav eluiga DM-i korral väheneb 10-15%.
DM põhjused on väga erinevad. Enamikul juhtudest areneb diabeet kas absoluutse insuliinipuuduse tagajärjel. (I tüüpi diabeet) CD-1) või perifeersete kudede insuliinitundlikkuse vähenemise tõttu koos pankrease β-rakkude sekretoorse düsfunktsiooniga. ( II tüüpi suhkurtõbi -. SD-2). Mõnel juhul on patsiendile DM-1 või DM-2 määramine keeruline, kuid praktikas on DM-i hüvitamine olulisem kui selle tüübi täpne määramine. Etioloogiline klassifikatsioon eristab nelja peamist diabeedi kliinilist klassi (tabel 7.1).
Enimlevinud DM-1 (jaotis 7.5), DM-2 (jaotis 7.6) ja gestatsiooniline DM (jaotis 7.9) on käsitletud eraldi peatükkides. Peal muud spetsiifilised liigid moodustab ainult umbes 1% DM juhtudest. Seda tüüpi DM-i etioloogiat ja patogeneesi näib olevat rohkem uuritud kui DM-1 ja eriti DM-2. Mitmed DM-i variandid on tingitud monogeensest pärilikkusest funktsiooni geneetilised defektidβ -rakud. See hõlmab autosomaalse domineerivalt päritud MODY sündroomi erinevaid variante (ingl. alanud noorte diabeet- täiskasvanute tüüpi diabeet noortel), mida iseloomustab rikkumine, kuid mitte insuliini sekretsiooni puudumine perifeersete kudede normaalse tundlikkusega selle suhtes.
Tab. 7.1. Diabeedi klassifikatsioon
Muide haruldane insuliini toime geneetilised defektid, seotud insuliiniretseptori mutatsiooniga (leprechaunism, Rabson-Mandehalli sündroom). DM areneb loomulikult koos eksokriinse kõhunäärme haigused, mis põhjustab β-rakkude hävimist (pankreatiit, pankreatektoomia, tsüstiline fibroos, hemokromatoos), aga ka mitmete endokriinsete haiguste korral, mille puhul esineb ülemäärane kontrainsulaarsete hormoonide tootmine (akromegaalia, Cushingi sündroom). Ravimid ja kemikaalid(Vacor, pentamidiin, nikotiinhape, diasoksiid jt) on harva DM põhjus, kuid võivad insuliiniresistentsusega inimestel kaasa aidata haiguse avaldumisele ja dekompensatsioonile. Rida nakkushaigused(punetised, tsütomegaalia, koksaki- ja adenoviiruse infektsioon) võib kaasneda β-rakkude hävimine, samas kui enamikul patsientidest määratakse CD-1 immunogeneetilised markerid. TO immuunvahendatud diabeedi haruldased vormid hõlmab diabeeti, mis areneb "jäik-rnani" sündroomiga (autoimmuunne neuroloogiline haigus) patsientidel, samuti diabeeti, mis on tingitud kokkupuutest insuliiniretseptorite vastaste autoantikehadega. Koos esinevad mitmesugused suurenenud sagedusega DM variandid
paljud geneetilised sündroomid, eriti Downi sündroomiga, Klinefelteri, Turneri, Wolframi, Prader-Willi ja paljude teistega.
7.2. SÜSIVESIKUTE AINEVAHETUSE FÜSIOLOOGIA KLIINILISED ASPEKTID
Insuliin sünteesitakse ja sekreteeritakse pankrease Langerhansi saarekeste (PZhZh) β-rakkude poolt. Lisaks eritavad Langerhansi saarekesed glükagooni (α-rakud), somatostatiini (δ-rakud) ja pankrease polüpeptiidi (PP-rakud). Saarerakkude hormoonid interakteeruvad üksteisega: glükagoon stimuleerib tavaliselt insuliini sekretsiooni ja somatostatiin pärsib insuliini ja glükagooni sekretsiooni. Insuliini molekul koosneb kahest polüpeptiidahelast (A-ahel - 21 aminohapet; B-ahel - 30 aminohapet) (joon. 7.1). Insuliini süntees algab preproinsuliini moodustumisega, mida proteaas lõhustab, moodustades proinsuliin. Golgi aparaadi sekretoorsetes graanulites lagundatakse proinsuliin insuliiniks ja C-peptiid, mis eksotsütoosi käigus verre erituvad (joon. 7.2).
Insuliini sekretsiooni peamine stimulaator on glükoos. Insuliin vabaneb vastusena vere glükoosisisalduse suurenemisele kahefaasiline(joonis 7.3). Esimene ehk äge faas kestab paar minutit ja see on seotud kogunenud vabanemisega
 Riis. 7.1. Insuliini molekuli primaarstruktuuri skeem
Riis. 7.1. Insuliini molekuli primaarstruktuuri skeem
 Riis. 7.2. Insuliini biosünteesi skeem
Riis. 7.2. Insuliini biosünteesi skeem
β-rakuline insuliin söögikordade vahelisel perioodil. Teine faas jätkub, kuni glükeemia tase saavutab normaalse tühja kõhuga (3,3-5,5 mmol / l). Sulfonüüluurea ravimid mõjutavad sarnaselt β-rakku.
Portaalisüsteemi kaudu jõuab insuliin maks- selle peamine sihtorgan. Maksa retseptorid seovad poole sekreteeritavast hormoonist. Teine pool, sattudes süsteemsesse vereringesse, jõuab lihastesse ja rasvkoesse. Suurem osa insuliinist (80%) läbib proteolüütilise lagunemise maksas, ülejäänud - neerudes ja ainult väike kogus metaboliseeritakse otse lihas- ja rasvarakkude poolt. Tavaline PZhZh
 Riis. 7.3. Insuliini kahefaasiline vabanemine glükoosi mõjul
Riis. 7.3. Insuliini kahefaasiline vabanemine glükoosi mõjul
täiskasvanu eritab 35-50 ühikut insuliini ööpäevas, mis on 0,6-1,2 ühikut 1 kg kehakaalu kohta. See sekretsioon jaguneb toiduks ja põhiliseks. toidu sekretsioon insuliin vastab söögijärgsele glükoositaseme tõusule, st. tänu sellele on tagatud toidu hüperglükeemilise toime neutraliseerimine. Toiduinsuliini kogus vastab ligikaudu sissevõetud süsivesikute kogusele - umbes 1-2,5 ühikut
10-12 g süsivesikute kohta (1 leivaühik - XE). Basaalinsuliini sekretsioon tagab optimaalse glükeemia ja anabolismi taseme söögikordade vahel ja une ajal. Basaalinsuliini eritub kiirusega umbes 1 U / h, pikaajalise füüsilise koormuse või pikaajalise tühja kõhuga väheneb see oluliselt. Toiduinsuliin moodustab vähemalt 50-70% päevasest insuliinitoodangust (joonis 7.4).
Insuliini sekretsioon ei sõltu mitte ainult toitumisest, vaid ka iga päev-
 Riis. 7 .4.
Päevase insuliinitootmise diagramm on normaalne
Riis. 7 .4.
Päevase insuliinitootmise diagramm on normaalne
kõikumised: insuliinivajadus tõuseb varajastel hommikutundidel ja siis päeva jooksul järk-järgult väheneb. Nii eritub hommikusöögiks 1 XE jaoks 2,0–2,5 U insuliini, lõunasöögiks 1,0–1,5 U ja õhtusöögiks 1,0 U. Selle insuliinitundlikkuse muutuse üheks põhjuseks on mitmete kontrainsulaarsete hormoonide (peamiselt kortisooli) kõrge tase hommikul, mis langeb öö hakul järk-järgult miinimumini.
Peamine insuliini füsioloogiline toime on glükoosi ülekande stimuleerimine insuliinist sõltuvate kudede rakumembraanide kaudu. Insuliini peamised sihtorganid on maks, rasvkude ja lihased. Insuliinist sõltumatud koed, mille varustamine glükoosiga ei sõltu insuliini toimest, hõlmavad eelkõige kesk- ja perifeerset närvisüsteemi, veresoonte endoteeli, vererakke jne. Insuliin stimuleerib glükogeeni sünteesi maksas ja lihastes, rasvade süntees maksas ja rasvkoes, valkude süntees maksas, lihastes ja teistes elundites. Kõik need muutused on suunatud glükoosi ärakasutamisele, mis viib selle taseme languseni veres. Insuliini füsioloogiline antagonist on glükagoon, mis stimuleerib glükogeeni ja rasvade mobiliseerimist depoost; Tavaliselt muutub glükagooni tase insuliini tootmisega vastastikku.
Insuliini bioloogilisi toimeid vahendab tema retseptorid asub sihtrakkudel. Insuliiniretseptor on glükoproteiin, mis koosneb neljast subühikust. Kõrge insuliinitasemega veres väheneb selle retseptorite arv vastavalt allareguleerimise põhimõttele, millega kaasneb raku tundlikkuse vähenemine insuliini suhtes. Pärast insuliini seondumist raku retseptoriga siseneb tekkinud kompleks rakku. Lihas- ja rasvarakkude sees põhjustab insuliin intratsellulaarsete vesiikulite mobilisatsiooni, mis sisaldavad glükoosi transportija GLUT-4. Selle tulemusena liiguvad vesiikulid raku pinnale, kus GLUT-4 toimib glükoosi sisselaskeavana. Sarnane tegevus GLUT-4 mõjutab treening.
7.3. DIABEEDI LABORATOORNE DIAGNOSTIKA JA HÜVITAMISKRITEERIUMID
Diabeedi laboratoorne diagnoos põhineb vere glükoosisisalduse määramisel, samas kui diagnostilised kriteeriumid on kõigile ühesugused.
SD tüübid ja variandid (tabel 7.2). Muude laboratoorsete uuringute (glükosuuria tase, glükeeritud hemoglobiini taseme määramine) andmeid ei tohi kasutada diabeedi diagnoosi kinnitamiseks. DM-i diagnoosi saab määrata kahe avastamise põhjal, millest üks kolm kriteeriumi:
1. Kell ilmsed sümptomid DM (polüuuria, polüdipsia) ja glükoosisisaldus täiskapillaarveres üle 11,1 mmol/l, sõltumata kellaajast ja eelmisest söögikorrast.
2. Kui glükoosi tase täiskapillaarveres on tühja kõhuga üle 6,1 mmol / l.
3. Kui glükoosisisaldus kapillaari täisveres on 2 tundi pärast 75 grammi glükoosi allaneelamist (suukaudne glükoositaluvuse test) üle 11,1 mmol / l.
Tab. 7.2. Diabeedi diagnoosimise kriteeriumid
 Kõige olulisem ja olulisem test diabeedi diagnoosimisel on tühja kõhu glükeemia taseme määramine (minimaalselt 8 tundi tühja kõhuga). Vene Föderatsioonis hinnatakse glükeemia taset reeglina täisveres. Glükoosi testimist kasutatakse laialdaselt paljudes riikides
Kõige olulisem ja olulisem test diabeedi diagnoosimisel on tühja kõhu glükeemia taseme määramine (minimaalselt 8 tundi tühja kõhuga). Vene Föderatsioonis hinnatakse glükeemia taset reeglina täisveres. Glükoosi testimist kasutatakse laialdaselt paljudes riikides
vereplasmas. Suukaudne glükoositaluvuse test(OGTT; glükoositaseme määramine 2 tundi pärast 75 grammi vees lahustatud glükoosi allaneelamist) omistatakse sellega seoses vähem tähtsust. OGTT põhjal aga diagnoositakse halvenenud glükoositaluvus(NTG). NTG diagnoositakse, kui tühja kõhu kapillaaride täisvere glükeemia tase ei ületa 6,1 mmol/l ja 2 tundi pärast glükoosikoormust on üle 7,8 mmol/l, kuid alla 11,1 mmol/l. Teine süsivesikute ainevahetuse häire variant on häiritud tühja kõhu glükeemia(NGNT). Viimane määratakse juhul, kui täiskapillaarvere glükeemia tase tühja kõhuga jääb vahemikku 5,6-6,0 mmol/l ja 2 tundi pärast glükoosikoormust on alla 7,8 mmol/l). NTG ja NGNT on praegu terminiga ühendatud prediabeet, kuna mõlemal patsiendikategoorial on kõrge risk diabeedi avaldumiseks ja diabeetilise makroangiopaatia tekkeks.
Diabeedi diagnoosimiseks tuleb glükeemia tase määrata standardsete laboratoorsete meetoditega. Glükeemiliste väärtuste tõlgendamisel tuleb meeles pidada, et tühja kõhu korral vastab täisveenivere glükoosisisaldus selle tasemele kapillaarveres. Pärast sööki ehk OGTT-d on selle tase veeniveres umbes 1,1 mmol/l madalam kui kapillaarveres. Plasma glükoosisisaldus on ligikaudu 0,84 mmol/l kõrgem kui täisveres. Hüvitise ja diabeediravi adekvaatsuse hindamiseks hinnatakse glükeemia taset kapillaarveres kaasaskantava seadme abil. glükomeetrid patsiendid ise, nende sugulased või meditsiinitöötajad.
Mis tahes tüüpi DM, aga ka märkimisväärse glükoosikoormuse korral, glükosuuria, mis on primaarsest uriinist glükoosi reabsorptsiooni läve ületamise tagajärg. Glükoosi reabsorptsiooni lävi on individuaalselt oluliselt erinev (≈ 9-10 mmol/l). Ühe näitajana ei tohiks glükosuuriat kasutada DM diagnoosimiseks. Tavaliselt glükosuuriat ei esine, välja arvatud olulise rafineeritud süsivesikute toidukoormuse korral.
Tooted ketoonkehad(atsetoon, atsetoatsetaat, β-hüdroksübutüraat) intensiivistub oluliselt absoluutse insuliinipuuduse korral. SD-1 dekompensatsiooniga on väljendunud ketonuuria(uurimisel kasutatakse testribasid, mis langevad uriini). Kerge (jälg)ketonuuria saab määrata tervetel inimestel nälgimise ja süsivesikutevaba dieedi ajal.
oluline labori näitaja, mida kasutatakse DM-i tüüpide diferentsiaaldiagnostikaks, samuti insuliinipuuduse tekke tuvastamiseks DM-2-ga patsientidel, on tase. C-peptiid. C-peptiidi tase veres võib kaudselt hinnata kõhunäärme β-rakkude insuliini sekretsioonivõimet. Viimased toodavad proinsuliini, millest enne sekretsiooni eraldatakse C-peptiid, mis siseneb verre insuliiniga võrdsetes kogustes. Insuliin on 50% ulatuses seotud maksas ja selle poolväärtusaeg perifeerses veres on umbes 4 minutit. Maks ei eemalda C-peptiidi vereringest ja selle poolväärtusaeg veres on umbes 30 minutit. Lisaks ei seondu see perifeeria raku retseptoritega. Seetõttu on C-peptiidi taseme määramine usaldusväärsem test saareaparaadi funktsioonide hindamiseks. C-peptiidi taset on kõige informatiivsem uurida stimulatsioonitestide taustal (pärast sööki või glükagooni manustamist). Test ei ole informatiivne, kui see viiakse läbi diabeedi raske dekompensatsiooni taustal, kuna raskel hüperglükeemial on toksiline toime β-rakkudele (glükoosi toksilisus). Insuliinravi eelnevatel päevadel ei mõjuta kuidagi testi tulemusi.
Põhiline ravi eesmärk Mis tahes tüüpi DM on selle hiliste tüsistuste ennetamine, mida on võimalik saavutada mitmete parameetrite stabiilse kompenseerimise taustal (tabel 7.3). Süsivesikute ainevahetuse kompenseerimise kvaliteedi peamine kriteerium DM-s on tase glükeeritud (glükosüülitud) hemoglobiin (HbA1c). Viimane on glükoosiga mittekovalentselt seotud hemoglobiin. Glükoos siseneb erütrotsüütidesse insuliinist sõltumatult ja hemoglobiini glükosüülimine on pöördumatu protsess ja selle aste on otseselt võrdeline glükoosi kontsentratsiooniga, millega see on 120 päeva jooksul kokkupuutes olnud. Väike osa hemoglobiinist on glükosüülitud ja normaalne; DM-iga saab seda oluliselt suurendada. HbA1c tase, erinevalt pidevalt muutuvast glükoositasemest, peegeldab lahutamatult glükeemiat viimase 3-4 kuu jooksul. Just selle intervalliga on soovitatav määrata HbA1c tase, et hinnata diabeedi kompensatsiooni.
Krooniline hüperglükeemia ei ole kaugeltki ainus riskitegur DM hiliste tüsistuste tekkeks ja progresseerumiseks. Selle tõttu DM hüvitise hindamine kompleksi põhjal
laboratoorsed ja instrumentaalsed uurimismeetodid (tabel 7.3). Lisaks süsivesikute ainevahetuse seisundit iseloomustavatele näitajatele on kõige olulisem vererõhu tase ja vere lipiidide spekter.
Tab. 7.3. Suhkurtõve hüvitamise kriteeriumid
 Lisaks ülaltoodud kompensatsioonikriteeriumidele on diabeedi ravi eesmärkide kavandamisel vajalik individuaalne lähenemine. DM-i hiliste komplikatsioonide (eriti mikroangiopaatia) tekke ja progresseerumise tõenäosus suureneb koos haiguse kestusega. Seega, kui lastel ja noortel patsientidel, kelle diabeedikogemus võib tulevikus ulatuda mitmekümne aastani, on vajalik saavutada optimaalne glükeemia, siis patsientidel, kellel DM avaldus vanemaealistel ja seniilses eas, jäik euglükeemiline kompensatsioon, mis suurendab oluliselt veresuhkru taset. hüpoglükeemia oht, mis ei ole alati asjakohane.
Lisaks ülaltoodud kompensatsioonikriteeriumidele on diabeedi ravi eesmärkide kavandamisel vajalik individuaalne lähenemine. DM-i hiliste komplikatsioonide (eriti mikroangiopaatia) tekke ja progresseerumise tõenäosus suureneb koos haiguse kestusega. Seega, kui lastel ja noortel patsientidel, kelle diabeedikogemus võib tulevikus ulatuda mitmekümne aastani, on vajalik saavutada optimaalne glükeemia, siis patsientidel, kellel DM avaldus vanemaealistel ja seniilses eas, jäik euglükeemiline kompensatsioon, mis suurendab oluliselt veresuhkru taset. hüpoglükeemia oht, mis ei ole alati asjakohane.
7.4. INSULIIN JA INSULIINRAAVI
Insuliinipreparaadid on 1. tüüpi diabeediga patsientidele üliolulised; lisaks saavad neid kuni 40% II tüüpi diabeediga patsientidest. Üldise juurde näidustused insuliinravi määramiseks diabeedi korral, millest paljud tegelikult kattuvad, hõlmavad järgmist:
1. 1. tüüpi diabeet
2. Pankreatektoomia
3. Ketoatsidootiline ja hüperosmolaarne kooma
4. II tüüpi diabeedi korral:
Insuliinipuuduse ilmsed nähud, nagu progresseeruv kaalulangus ja ketoos, raske hüperglükeemia;
Suured kirurgilised sekkumised;
Ägedad makrovaskulaarsed tüsistused (insult, müokardiinfarkt, gangreen jne) ja rasked nakkushaigused, millega kaasneb süsivesikute metabolismi dekompensatsioon;
Tühja kõhu glükeemia tase on üle 15-18 mmol / l;
Stabiilse hüvitise puudumine, hoolimata erinevate tablettide hüpoglükeemiliste ravimite maksimaalsete ööpäevaste annuste määramisest;
Diabeedi hiliste komplikatsioonide hilised staadiumid (raske polüneuropaatia ja retinopaatia, krooniline neerupuudulikkus).
5. Suutmatus saavutada dieetravi abil rasedusdiabeedi kompensatsiooni.
Päritolu Insuliinipreparaadid võib jagada kolme rühma:
loomsed insuliinid (sealiha);
Inimese insuliinid (poolsünteetilised, geneetiliselt muundatud);
Insuliini analoogid (lispro, aspart, glargiin, detemiir).
Iniminsuliini tootmise tehnoloogia areng on viinud selleni, et kasutatakse sea insuliin(erineb inimese omast ühe aminohappe poolest) Hiljuti oluliselt vähenenud. Sealiha insuliini saab kasutada iniminsuliini valmistamiseks poolsünteetiline meetod, mis hõlmab ühe erineva aminohappe asendamist selle molekulis. Kõrgeima kvaliteediga on geenitehnoloogia iniminsuliinid. Nende saamiseks seostatakse genoomiga inimese genoomi piirkond, mis vastutab insuliini sünteesi eest E. coli või pärmikultuuri, mille tulemusena hakkavad viimased tootma humaaninsuliini. Loomine insuliini analoogid erinevate aminohapete permutatsioonide abil oli eesmärgiks saada etteantud ja soodsaima farmakokineetikaga ravimeid. Niisiis, insuliin lispro (Humalog) on analoog
ülilühiajalise toimega insuliin, mille hüpoglükeemiline toime avaldub juba 15 minutit pärast süstimist. Seevastu insuliini analoogi glargiini (Lantus) iseloomustab pikaajaline toime, mis kestab kogu päeva, samas kui ravimi kineetikat iseloomustab plasmakontsentratsiooni väljendunud piikide puudumine. Enamik praegu kasutatavaid insuliinipreparaate ja selle analooge on toodetud aastal kontsentratsioon 100 U/ml. Kõrval toime kestus insuliinid jagunevad 4 põhirühma (tabel 7.4):
Tab. 7.4. Ravimite ja insuliini analoogide farmakokineetika
 1.
Ultralühiajaline toime (lispro, aspart).
1.
Ultralühiajaline toime (lispro, aspart).
2. Lühitoimeline (lihtne iniminsuliin).
3. Keskmine toimeaeg (insuliinid neutraalsel protamiinil Hagedorn).
4. Pikatoimeline (glargiin, detemiir).
5. Erineva toimeajaga insuliinide segud (Novomix-30, Humulin-MZ, Humalog-Mix-25).
Ettevalmistused ülilühike tegevus[lispro (Humalog), aspart (Novorapid)] on insuliini analoogid. Nende eelised on hüpoglükeemilise toime kiire areng pärast süstimist (pärast 15 minutit), mis võimaldab süstimist vahetult enne sööki või isegi vahetult pärast sööki, samuti lühike toimeaeg (alla 3 tunni), mis vähendab hüpoglükeemia riski. . Ettevalmistused lühike tegevus(lihtinsuliin, tavaline insuliin) on lahus, mis sisaldab insuliini kontsentratsioonis 100 U / ml. Lihtne insuliinisüst tehakse 30 minutit enne sööki; toime kestus on umbes 4-6 tundi. Ultralühi- ja lühitoimelisi preparaate võib manustada subkutaanselt, intramuskulaarselt ja intravenoosselt.
Narkootikumide hulgas keskmise kestusega tegevused neutraalse protamiini Hagedorn (NPH) kõige sagedamini kasutatavad preparaadid. NPH on valk, mis adsorbeerib insuliini mittekovalentselt, aeglustades selle imendumist nahaalusest depoost. NPH-insuliinide efektiivne toimeaeg on tavaliselt umbes 12 tundi; neid manustatakse ainult subkutaanselt. NPH-insuliin on suspensioon ja seetõttu on see erinevalt tavainsuliinist viaalis hägune ja pikaajalisel seismisel moodustub suspensioon, mida tuleb enne süstimist põhjalikult segada. Erinevalt teistest pikatoimelistest ravimitest võib NPH-insuliine segada mis tahes vahekorras lühitoimelise insuliiniga (lihtinsuliiniga), samas kui segu komponentide farmakokineetika ei muutu, kuna NPH ei seo täiendavaid koguseid lihtinsuliini ( joon. 7.5). Lisaks kasutatakse protamiini insuliini analoogide (Novomix-30, Humalog-Mix-25) standardsete segude valmistamiseks.
Pikatoimeliste ravimite hulgas kasutatakse praegu aktiivselt insuliini analooge. glargiin(Lantus) ja detemir(Levemir). Nende ravimite farmakokineetika eeliseks on see, et erinevalt NPH-insuliinidest tagavad nad ühtlasema ja pikemaajalisema ravimi sissevõtmise nahaalusest depoost. Sellega seoses võib glargiini manustada ainult üks kord päevas ja peaaegu sõltumata kellaajast.
 Riis. 7.5. Erinevate insuliinipreparaatide farmakokineetika:
Riis. 7.5. Erinevate insuliinipreparaatide farmakokineetika:
a) ühekomponentne; b) insuliinide standardsed segud
Lisaks monokomponentsetele insuliinipreparaatidele kasutatakse kliinilises praktikas laialdaselt standardsed segud. Reeglina räägime lühikese või ülilühikese insuliini segudest keskmise toimeajaga insuliiniga. Näiteks ravim "Humulin-MZ" sisaldab ühes viaalis 30% lihtsat insuliini ja 70% NPH insuliini; Novomix-30 sisaldab 30% aspartinsuliini ja 70% aspartinsuliini kristalset protamiini suspensiooni; Humalog-Mix-25 sisaldab 25% insuliin lispro ja 75% insuliin lispro protamiini suspensiooni. eelis
standardsed insuliinisegud on kahe süsti asendamine ühega ja segu komponentide annuste mõnevõrra suurem täpsus; puuduseks on segu üksikute komponentide individuaalse doseerimise võimatus. See määrab eelistuse standardsete insuliinisegude kasutamiseks DM-2 raviks või koos nn traditsiooniline insuliinravi(insuliini fikseeritud annuste määramine), samas kui intensiivne insuliinravi(paindlik annuse valik sõltuvalt glükeemilistest näitajatest ja süsivesikute kogusest toidus), eelistatav on ühekomponentsete preparaatide kasutamine.
Eduka insuliinravi võti on selle range järgimine süstimistehnikad. Insuliini manustamiseks on mitu võimalust. Lihtsaim ja samal ajal usaldusväärsem meetod on insuliini süstimine süstal. Mugavam viis insuliini manustamiseks on süstid. süstla pliiatsid, mis on kombineeritud seade, mis sisaldab insuliini reservuaari (padrunit), doseerimissüsteemi ja nõela koos injektoriga.
Säilitusraviks (kui me ei räägi diabeedi raskest dekompensatsioonist või kriitilistest seisunditest) manustatakse insuliini subkutaanselt. Lühitoimelist insuliini soovitatakse süstida kõhupiirkonna nahaalusesse rasvkoesse, pikatoimelist insuliini - reie- või õlakudedesse (joonis 7.6 a). Süstid tehakse sügavale nahaalusesse koesse läbi laialt kokkusurutud naha 45° nurga all (joonis 7.6 b). Patsienti tuleb soovitada vahetada igapäevaseid insuliini süstekohti samas piirkonnas, et vältida lipodüstroofia teket.
TO tegurid, mis mõjutavad insuliini imendumise kiirust subkutaansest depoost tuleb omistada insuliini annus (annuse suurendamine pikendab imendumise kestust), süstekoht (kõhukoest imendub kiiremini), ümbritseva õhu temperatuur (soojendamine ja süstekoha masseerimine kiirendab imendumist).
Keerulisem manustamisviis, mis aga võimaldab paljudel patsientidel saavutada häid ravitulemusi, on kasutamine insuliini dosaator, või süsteemid insuliini pidevaks subkutaanseks manustamiseks. Dosaator on kaasaskantav seade, mis koosneb arvutist, mis määrab insuliini manustamisrežiimi, samuti insuliini manustamissüsteemist kateetri ja miniatuurse hüpodermilise nõela kaudu.
 Riis. 7.6. Insuliini süstid: a) tüüpilised süstekohad; b) insuliinisüstla nõela asukoht süstimise ajal
Riis. 7.6. Insuliini süstid: a) tüüpilised süstekohad; b) insuliinisüstla nõela asukoht süstimise ajal
rasvkude. Dosaatori abil viiakse läbi lühitoimelise või ülilühitoimelise insuliini pidev põhimanustamine (kiirus suurusjärgus 0,5-1 U / tund) ja enne söömist, sõltuvalt süsivesikute sisaldusest selles. ja glükeemia taset, süstib patsient sama lühitoimelise insuliini vajaliku boolusannuse. Dosaatoriga insuliinravi eeliseks on ainult lühitoimelise (või isegi ülilühikese) insuliini kasutuselevõtt, mis iseenesest on mõnevõrra füsioloogilisem, kuna pikaajaliste insuliinipreparaatide imendumine on suurte kõikumiste all; sellega seoses on lühitoimelise insuliini pidev manustamine paremini juhitav. Dosaatoriga insuliinravi puuduseks on vajadus seadet pidevalt kanda, samuti süstenõela pikk viibimine nahaalune kude mis nõuavad insuliinivarustuse protsessi perioodilist jälgimist. Dosaatorit kasutav insuliinravi on eelkõige näidustatud I tüüpi diabeediga patsientidele, kes on valmis selle manustamistehnikat valdama. Eelkõige tuleks sellega seoses tähelepanu pöörata patsientidele, kellel on väljendunud koidiku nähtus, samuti rasedatele ja rasedust planeerivatele DM-1-ga patsientidele ning patsientidele.
Korraliku eluviisiga entid (paindlikuma toitumise võimalus).
7.5. 1. TÜÜPI DIABEET
CD-1 - elundispetsiifiline autoimmuunne haigus, mis põhjustab kõhunäärme saarekeste insuliini tootvate β-rakkude hävimist, mis väljendub insuliini absoluutses puuduses. Mõnel juhul ei ole ilmse DM-1-ga patsientidel β-rakkude autoimmuunse kahjustuse markereid. (idiopaatiline CD-1).
Etioloogia
CD-1 on haigus, millel on pärilik eelsoodumus, kuid selle panus haiguse arengusse on väike (määrab selle arengu umbes 1/3 võrra). CD-1 identsete kaksikute vastavus on ainult 36%. Tõenäosus haigestuda DM-1 lapsel, kellel on haige ema, on 1-2%, isa - 3-6%, vend või õde - 6%. Üks või mitu autoimmuunse β-rakkude kahjustuse humoraalset markerit, mis hõlmavad pankrease saarekeste antikehi, glutamaadi dekarboksülaasi (GAD65) ja türosiinfosfataasi (IA-2 ja ΙΑ-2β) vastaseid antikehi, on leitud 85–90% juhtudest. patsiendid. Sellegipoolest on rakulise immuunsuse tegurid β-rakkude hävitamisel esmatähtsad. CD-1 on seotud selliste HLA haplotüüpidega nagu DQA Ja DQB, samas kui mõned alleelid HLA-DR/DQ võivad soodustada haiguse arengut, samas kui teised on kaitsvad. Suurenenud sagedusega kombineeritakse CD-1 teiste autoimmuunsete endokriinsete (autoimmuunne türeoidiit, Addisoni tõbi) ja mitte-endokriinsete haigustega, nagu alopeetsia, vitiliigo, Crohni tõbi, reumaatilised haigused (tabel 7.5).
Patogenees
CD-1 avaldub siis, kui autoimmuunprotsessi käigus hävib 80-90% β-rakkudest. Selle protsessi kiirus ja intensiivsus võivad oluliselt erineda. Kõige sagedamini siis, kui tüüpiline vool laste ja noorte haiguste puhul kulgeb see protsess üsna kiiresti, millele järgneb haiguse kiire ilming, mille puhul esimeste kliiniliste sümptomite ilmnemisest ketoatsidoosi tekkeni (kuni ketoatsidootilise koomani) võib mööduda vaid mõni nädal.
Tab. 7.5. 1. tüüpi diabeet
 Tabeli jätk. 7.5
Tabeli jätk. 7.5
 Muudel, palju harvematel juhtudel, tavaliselt üle 40-aastastel täiskasvanutel, võib haigus olla varjatud. (latentne autoimmuunne diabeet täiskasvanutel – LADA), samal ajal diagnoositakse sellistel patsientidel haiguse alguses sageli DM-2 ja mitme aasta jooksul saab DM-i kompenseerida sulfonüüluurea ravimite määramisega. Kuid tulevikus, tavaliselt 3 aasta pärast, ilmnevad absoluutse insuliinipuuduse tunnused (kaalulangus, ketonuuria, raske hüperglükeemia, hoolimata hüpoglükeemiliste tablettide võtmisest).
Muudel, palju harvematel juhtudel, tavaliselt üle 40-aastastel täiskasvanutel, võib haigus olla varjatud. (latentne autoimmuunne diabeet täiskasvanutel – LADA), samal ajal diagnoositakse sellistel patsientidel haiguse alguses sageli DM-2 ja mitme aasta jooksul saab DM-i kompenseerida sulfonüüluurea ravimite määramisega. Kuid tulevikus, tavaliselt 3 aasta pärast, ilmnevad absoluutse insuliinipuuduse tunnused (kaalulangus, ketonuuria, raske hüperglükeemia, hoolimata hüpoglükeemiliste tablettide võtmisest).
Nagu mainitud, on DM-1 patogeneesi keskmes absoluutne insuliinipuudus. Glükoosi sisenemise võimatus insuliinist sõltuvatesse kudedesse (rasv ja lihased) põhjustab energiapuudust, mille tagajärjel intensiivistuvad lipolüüs ja proteolüüs, mis on seotud kehakaalu langusega. Glükeemia taseme tõus põhjustab hüperosmolaarsust, millega kaasneb osmootne diurees ja tõsine dehüdratsioon. Insuliinipuuduse ja energiapuuduse tingimustes pärsitakse kontrainsulaarsete hormoonide (glükagoon, kortisool, kasvuhormoon) tootmine, mis hoolimata suurenevast glükeemiast põhjustab glükoneogeneesi stimuleerimist. Suurenenud lipolüüs rasvkoes toob kaasa vabade kontsentratsiooni olulise suurenemise rasvhapped. Insuliinipuuduse korral on maksa liposünteesivõime pärsitud ja vaba
nye rasvhapped hakkavad sisalduma ketogeneesis. Ketoonkehade kuhjumine põhjustab diabeetilise ketoosi ja hiljem ketoatsidoosi arengut. Dehüdratsiooni ja atsidoosi progresseeruva suurenemisega tekib kooma (vt lõik 7.7.1), mis insuliinravi ja rehüdratsiooni puudumisel lõpeb paratamatult surmaga.
Epidemioloogia
DM-1 moodustab ligikaudu 1,5-2% kõigist diabeedijuhtudest ja see suhteline arv väheneb jätkuvalt DM-2 esinemissageduse kiire kasvu tõttu. Eluaegne risk haigestuda CD-1 valge rassi puhul on umbes 0,4%. DM-1 esinemissagedus kasvab 3% aastas: 1,5% uute juhtude tõttu ja veel 1,5% patsientide eluea pikenemise tõttu. CD-1 levimus varieerub sõltuvalt elanikkonna etnilisest koosseisust. 2000. aasta seisuga oli see Aafrikas 0,02%, Lõuna-Aasias ning Lõuna- ja Kesk-Ameerikas 0,1% ning Euroopas ja Põhja-Ameerikas 0,2%. Kõige suurem on DM-1 esinemissagedus Soomes ja Rootsis (30-35 juhtu 100 tuhande elaniku kohta aastas), madalaim Jaapanis, Hiinas ja Koreas (vastavalt 0,5-2,0 juhtu). CD-1 manifestatsiooni vanuse tippaeg on ligikaudu 10-13 aastat. Enamikul juhtudest avaldub CD-1 enne 40. eluaastat.
Kliinilised ilmingud
IN tüüpilised juhtumid eriti lastel ja noortel debüteerib CD-1 erksa kliinilise pildiga, mis areneb mitme kuu või isegi nädala jooksul. CD-1 manifestatsiooni võivad provotseerida nakkus- ja muud kaasuvad haigused. Iseloomulik kõikidele diabeeditüüpidele omased sümptomid, seotud hüperglükeemiaga: polüdipsia, polüuuria, sügelus, kuid SD-1 puhul on need väga väljendunud. Seega saavad patsiendid kogu päeva jooksul juua ja eritada kuni 5-10 liitrit vedelikku. spetsiifiline DM-1 puhul on absoluutsest insuliinipuudusest põhjustatud sümptomiks kaalulangus, mis jõuab 1-2 kuu jooksul 10-15 kg-ni. Iseloomulik on väljendunud üldine ja lihasnõrkus, töövõime langus, unisus. Haiguse alguses võib mõnel patsiendil tekkida söögiisu suurenemine, mis ketoatsidoosi tekkimisel asendub anoreksiaga. Viimast iseloomustab atsetoonilõhna (või puuviljalõhna) ilmumine suust,
märkus, oksendamine, sageli kõhuvalu (pseudoperitoniit), tugev dehüdratsioon ja lõpeb kooma tekkega (vt punkt 7.7.1). Mõnel juhul on CD-1 esimene ilming lastel progresseeruv teadvuse kahjustus kuni koomani kaasuvate haiguste, tavaliselt nakkusliku või ägeda kirurgilise patoloogia taustal.
Suhteliselt harvadel juhtudel on CD-1 arenemine üle 35-40-aastastel inimestel (varjatud autoimmuunne diabeet täiskasvanutel) haigus ei pruugi avalduda nii selgelt (mõõdukas polüdipsia ja polüuuria, kaalulangus puudub) ja seda avastada isegi juhuslikult glükeemia taseme rutiinsel määramisel. Nendel juhtudel diagnoositakse patsiendil sageli alguses DM-2 ja ta määrab suukaudsed hüpoglükeemilised ravimid (TSP), mis mõneks ajaks pakuvad DM-i vastuvõetavat kompensatsiooni. Kuid mitme aasta jooksul (sageli aasta jooksul) tekivad patsiendil süveneva absoluutse insuliinipuuduse tõttu sümptomid: kehakaalu langus, võimetus säilitada normaalset glükeemiat TSP taustal, ketoos, ketoatsidoos.
Diagnostika
Arvestades, et DM-1-l on elav kliiniline pilt ja see on ka suhteliselt haruldane haigus, ei ole DM-1 diagnoosimiseks glükeemia taseme skriiningmääramine näidustatud. Tõenäosus haigestuda haigestunute lähedastele on väike, mis koos tõhusate meetodite puudumisega esmane ennetus CD-1 määrab nendes haiguse immunogeneetiliste markerite uurimise sobimatuse. DM-1 diagnoos põhineb enamikul juhtudest olulise hüperglükeemia tuvastamisel patsientidel, kellel on absoluutse insuliinipuuduse rasked kliinilised ilmingud. OGTT-d DM-1 diagnoosimiseks tuleb teha väga harva.
Kahtlastel juhtudel (keskmise raskusega hüperglükeemia tuvastamine ilmsete kliiniliste ilmingute puudumisel, manifestatsioon suhteliselt keskeas), samuti diferentsiaaldiagnoosimiseks teiste DM-i tüüpidega, taseme määramine. C-peptiid(basaal ja 2 tundi pärast sööki). kaudne diagnostiline väärtus kahtlastel juhtudel võib olla määratlus immunoloogilised markerid CD-1 - saarekeste antikehad
PZhZh, glutamaadi dekarboksülaasi (GAD65) ja türosiinfosfataasi (IA-2 ja IA-2β) jaoks. CD-1 ja CD-2 diferentsiaaldiagnoos on esitatud tabelis. 7.6.
Tab. 7.6. Diferentsiaaldiagnoos ja erinevused CD-1 ja CD-2 vahel
 Ravi
Ravi
Mis tahes tüüpi DM-i ravi põhineb kolmel põhiprintsiibil: hüpoglükeemiline ravi (DM-1 korral - insuliinravi), dieet ja patsiendi koolitus. insuliinravi SD-1 kuludega asendamine ja selle eesmärk on maksimaalselt imiteerida hormooni füsioloogilist tootmist, et saavutada aktsepteeritud kompensatsioonikriteeriumid (tabel 7.3). Füsioloogilisele insuliini sekretsioonile kõige lähemal intensiivne insuliinravi. Insuliinivajadus, mis vastab selle basaalsekretsioon, varustatud kahe keskmise toimeajaga insuliini süstiga (hommikul ja õhtul) või ühe pikatoimelise insuliini (glargiini) süstiga. Basaalinsuliini koguannus
rida ei tohiks ületada poolt ravimi ööpäevasest koguvajadusest. Insuliini sekretsioon söögi ajal või boolusena asendatakse lühikese või ülikiire insuliini süstimisega enne iga sööki, samas kui selle annus arvutatakse eelseisva söögikorra ajal eeldatavalt tarbitavate süsivesikute koguse ja patsiendi poolt glükomeetri abil kindlaks määratud veresuhkru taseme alusel. enne iga insuliinisüsti (joonis 7.7).
Hinnanguline intensiivne insuliinirežiim, mis muutub peaaegu iga päev, võib kujutada järgmiselt. Eeldatakse, et päevane insuliinivajadus on umbes 0,5–0,7 U 1 kg kehakaalu kohta (70 kg kaaluva patsiendi puhul umbes 35–50 U). Umbes 1/s–1/2 sellest annusest moodustab pikatoimeline insuliin (20–25 U), 1/2–2/s lühitoimeline või ülilühitoimeline insuliin. NPH-insuliini annus jagatakse 2 süstiks: hommikul 2 / s selle annusest (12 U), õhtul - 1 / s (8-10 U).
eesmärk esimene aste Insuliinravi valik on tühja kõhuga glükoositaseme normaliseerimine. NPH-insuliini õhtune annus manustatakse tavaliselt kell 20-23, millele järgneb hommikune lühitoimelise insuliini annus enne hommikusööki. NPH insuliini õhtuse annuse valimisel tuleb silmas pidada võimalust, et tekib mitmeid
 Riis. 7.7. Intensiivse insuliinravi skeem
Riis. 7.7. Intensiivse insuliinravi skeem
üsna tüüpilised nähtused. Hommikuse hüperglükeemia põhjuseks võib olla pikatoimelise insuliini ebapiisav annus, kuna hommikuks suureneb insuliinivajadus märkimisväärselt ("koidu" fenomen). Lisaks annuse ebapiisavale annusele võib selle liig põhjustada hommikust hüperglükeemiat - Somoji fenomen(Somogyi), posthüpoglükeemiline hüperglükeemia. Seda nähtust seletatakse asjaoluga, et kudede maksimaalne tundlikkus insuliini suhtes toimub kella 2–4 vahel öösel. Just sel ajal on peamiste kontrainsulaarsete hormoonide (kortisool, kasvuhormoon jne) tase tavaliselt madalaim. Kui pikatoimelise insuliini õhtune annus on ülemäärane, siis sel ajal areneb hüpoglükeemia. Kliiniliselt võib see ilmneda halva unena koos õudusunenägude, teadvuseta unetegevuse, hommikuste peavalude ja väsimusega. Hüpoglükeemia tekkimine põhjustab sel ajal glükagooni ja teiste kontrainsulaarsete hormoonide märkimisväärset kompenseerivat vabanemist, millele järgneb hüperglükeemia hommikul. Kui sellises olukorras prolongeeritult manustatava insuliini annust ei vähendata, vaid suurendatakse, süvenevad öine hüpoglükeemia ja hommikune hüperglükeemia, mis võib lõpuks viia kroonilise insuliini üleannustamise sündroomini (Somogyi sündroom), mis on kombinatsioon rasvumisest ja. diabeedi krooniline dekompensatsioon, sagedane hüpoglükeemia ja progresseeruvad hilised tüsistused. Somogyi fenomeni diagnoosimiseks on vaja uurida glükeemia taset umbes kell 3 öösel, mis on insuliinravi valiku lahutamatu osa. Kui langus õhtul NPH annused Et öise hüpoglükeemia tekke seisukohast ohutuks kaasneb hommikune hüperglükeemia (koidu nähtus), tuleb patsiendil soovitada tõusta varem (6-7 hommikul), samal ajal, kui insuliini manustatakse öösel. säilitab endiselt normaalse glükeemia taseme.
Teine NPH-insuliini süst tehakse tavaliselt enne hommikusööki koos lühitoimelise (ülilühiajalise) insuliinisüstiga hommikul. Sel juhul valitakse annus peamiselt glükeemia taseme näitajate põhjal enne peamisi igapäevaseid söögikordi (lõunasöök, õhtusöök); lisaks võib seda piirata hüpoglükeemia tekkimine söögikordade vahel, näiteks keskpäeval, hommiku- ja lõunasöögi vahel.
Terve annus insuliini pikaajaline tegevus(glargiini) manustatakse üks kord päevas, pole vahet, mis kell. Kineetika
glargiin- ja detemirinsuliinid on hüpoglükeemia, sealhulgas öise hüpoglükeemia tekkeriski seisukohalt soodsamad.
Lühi- või ülilühitoimelise insuliini annus sõltub isegi patsiendi insuliini manustamise esimesel päeval tarbitud süsivesikute (leivaühikute) kogusest ja glükeemia tasemest enne süstimist. Tavaliselt võetakse õhtusöögiks umbes 1/4 annusest lühitoimelist insuliini (6-8 RÜ), lähtudes insuliini sekretsiooni päevasest rütmist normis, ülejäänud annus jagatakse ligikaudu võrdselt hommiku- ja lõunasöögiks (10-12). RÜ). Mida kõrgem on glükeemia algtase, seda vähem see manustatud insuliiniühiku kohta väheneb. Lühitoimelist insuliini manustatakse 30 minutit enne sööki, ülilühitoimelist insuliini vahetult enne sööki või isegi vahetult pärast sööki. Lühitoimelise insuliini annuse piisavust hinnatakse glükeemianäitajate järgi 2 tundi pärast sööki ja enne järgmist söögikorda.
Insuliini annuse arvutamiseks intensiivse insuliinravi ajal piisab XE arvu arvutamisest ainult süsivesikute komponendi põhjal. Samas ei lähe arvesse mitte kõik süsivesikuid sisaldavad tooted, vaid ainult nn loendatavad. Viimaste hulka kuuluvad kartul, teraviljatooted, puuviljad, vedelad piimatooted ja suhkrurikkad toidud. Arvesse ei võeta tooteid, mis sisaldavad mitteseeditavaid süsivesikuid (enamik köögivilju). Välja on töötatud spetsiaalsed vahetustabelid, mille abil süsivesikute kogust XE-s väljendades on võimalik välja arvutada vajalik insuliiniannus. Üks XE vastab 10-12 g süsivesikutele (tabel 10.7).
Pärast 1 XE-d sisaldavat sööki tõuseb glükeemia tase 1,6-2,2 mmol / l, s.o. umbes sama palju kui glükoosi tase väheneb 1 ühiku insuliini sisestamisel. Teisisõnu, iga toidus sisalduva XU kohta, mida kavatsetakse süüa, on vaja eelnevalt manustada (olenevalt kellaajast) umbes 1 ühik insuliini. Lisaks tuleb arvesse võtta glükeemia taseme enesekontrolli tulemusi, mis tehakse enne iga süsti, ja kellaaega (umbes 2 RÜ insuliini 1 XE kohta hommikul ja lõuna ajal, 1 RÜ 1 XE kohta õhtusöögiks). Seega, kui tuvastatakse hüperglükeemia, tuleb insuliini annust, mis arvutatakse vastavalt eelseisvale söögikorrale (vastavalt XE arvule), suurendada ja vastupidi, kui tuvastatakse hüpoglükeemia, manustatakse vähem insuliini.
Tab. 7.7. 1 XE moodustavate toodete samaväärne asendamine
 Näiteks kui patsiendil on 30 minutit enne planeeritud 5 XE-d sisaldavat õhtusööki glükeemiline tase 7 mmol/l, peab ta süstima 1 ühiku insuliini, et glükeemia langeks. normaalne tase: 7 mmol/l kuni umbes 5 mmol/l. Lisaks tuleb 5 XE katmiseks manustada 5 ühikut insuliini. Seega süstib patsient sel juhul 6 ühikut lühitoimelist või ülikiiret insuliini.
Näiteks kui patsiendil on 30 minutit enne planeeritud 5 XE-d sisaldavat õhtusööki glükeemiline tase 7 mmol/l, peab ta süstima 1 ühiku insuliini, et glükeemia langeks. normaalne tase: 7 mmol/l kuni umbes 5 mmol/l. Lisaks tuleb 5 XE katmiseks manustada 5 ühikut insuliini. Seega süstib patsient sel juhul 6 ühikut lühitoimelist või ülikiiret insuliini.
Pärast CD-1 avaldumist ja insuliinravi alustamist piisavalt pikka aega võib insuliinivajadus olla väike ja olla väiksem kui 0,3-0,4 U / kg. Seda perioodi nimetatakse remissioonifaasiks või "Mesinädalad". Pärast hüperglükeemia ja ketoatsidoosi perioodi, mis pärsivad insuliini sekretsiooni 10-15% ülejäänud β-rakkudest, taastab hormonaalsete ja ainevahetushäirete kompenseerimine insuliini manustamisega nende rakkude funktsiooni, mis seejärel võtavad üle keha insuliiniga minimaalsel tasemel. See periood võib kesta mitu nädalat kuni mitu aastat, kuid lõpuks saab "mesinädalad" allesjäänud β-rakkude autoimmuunse hävimise tõttu läbi.
Dieet DM-1-ga treenitud patsientidel, kellel on enesekontrolli ja insuliiniannuse valiku oskused, saab seda liberaliseerida, s.t. läheneb vabaks. Kui patsient ei ole ülekaaluline või alakaaluline, peaks dieet olema
isokaloriline. DM-1 toidu põhikomponent on süsivesikud, mis peaksid moodustama umbes 65% päevasest kalorist. Eelistada tuleks toiduaineid, mis sisaldavad kompleksseid, aeglaselt imenduvaid süsivesikuid, aga ka kiudainerikkaid toite. Vältida tuleks kergesti seeditavaid süsivesikuid sisaldavaid toite (jahu, magus). Valkude osakaalu tuleks vähendada 10-35%-ni, mis aitab vähendada mikroangiopaatia tekkeriski ja rasvade osakaalu 25-35%-ni, samas kui rasvade piiramine peaks moodustama kuni 7% kaloritest, mis vähendab ateroskleroosi tekke oht. Lisaks peaksite vältima võtmist alkohoolsed joogid eriti tugevad.
DM-1-ga patsiendiga töötamise lahutamatu osa ja selle tõhusa hüvitamise võti on patsiendi koolitus. Patsient peab kogu elu jooksul iseseisvalt muutma insuliini annust iga päev, sõltuvalt paljudest teguritest. Ilmselgelt eeldab see teatud oskuste omamist, mida patsiendile tuleb õpetada. "SD-1 patsiendi kool" korraldatakse endokrinoloogiahaiglates või ambulatoorsetes haiglates ja koosneb 5-7 struktureeritud sessioonist, mille käigus arst või eriväljaõppe saanud õde õpetab interaktiivses režiimis, kasutades erinevaid visuaalseid abivahendeid, patsientidele põhimõtteid enesekontroll.
Prognoos
Insuliinravi puudumisel sureb DM-1-ga patsient paratamatult ketoatsidootilise kooma tõttu. Ebapiisava insuliinravi korral, mille korral ei ole täidetud diabeedi kompenseerimise kriteeriumid ja patsient on kroonilises hüperglükeemias (tabel 7.3), hakkavad arenema ja progresseeruma hilised tüsistused (punkt 7.8). DM-1 puhul on diabeetilise mikroangiopaatia (nefropaatia ja retinopaatia) ja neuropaatia (diabeetilise jala sündroom) ilmingud selles osas suurima kliinilise tähtsusega. Makroangiopaatia DM-1 puhul tuleb esile suhteliselt harva.
7.6. 2. TÜÜP DIABEET
2. tüüpi diabeet- krooniline haigus, mis väljendub süsivesikute metabolismi rikkumises koos hüperglükeemia tekkega insuliiniresistentsuse ja β-rakkude sekretoorse düsfunktsiooni tõttu;
samuti lipiidide metabolismi ateroskleroosi tekkega. Kuna patsientide surma ja puude peamine põhjus on süsteemse ateroskleroosi tüsistused, nimetatakse CD-2 mõnikord ka südame-veresoonkonna haiguseks.
Tab. 7.8. 2. tüüpi diabeet
 Etioloogia
Etioloogia
CD-2 on päriliku eelsoodumusega multifaktoriaalne haigus. Identsete kaksikute CD-2 vastavus ulatub 80% -ni või rohkem. Enamik CD-2-ga patsiente viitab CD-2 esinemisele lähisugulaste seas; CD-2 olemasolul ühel vanemal on selle arengu tõenäosus järglastel kogu elu jooksul 40%. Ühtegi geeni, mille polümorfism määrab CD-2 eelsoodumuse, pole leitud. CD-2 päriliku eelsoodumuse rakendamisel mängivad suurt tähtsust keskkonnategurid, peamiselt elustiili tunnused. CD-2 arengu riskitegurid on:
Rasvumine, eriti vistseraalne (vt lõik 11.2);
etnilisus (eriti traditsioonilise eluviisi muutmisel läänelikule);
Istuv eluviis;
Toitumisspetsiifika (suur rafineeritud süsivesikute tarbimine ja madal sisaldus kiudained);
Arteriaalne hüpertensioon.
Patogenees
Patogeneetiliselt on CD-2 heterogeenne metaboolsete häirete rühm ja just see määrab selle olulise kliinilise heterogeensuse. Selle patogenees põhineb insuliiniresistentsusel (insuliini vahendatud glükoosi kasutamise vähenemine kudedes), mis realiseerub β-rakkude sekretoorse düsfunktsiooni taustal. Seega on insuliinitundlikkuse ja insuliini sekretsiooni vahel tasakaalustamatus. Sekretsiooni düsfunktsioonβ -rakud See seisneb insuliini "varajase" sekretoorse vabanemise aeglustamises vastusena vere glükoositaseme tõusule. Samal ajal praktiliselt puudub sekretsiooni 1. (kiire) faas, mis seisneb vesiikulite tühjendamises kogunenud insuliiniga; Sekretsiooni 2. (aeglane) faas viiakse läbi vastusena stabiliseerivale hüperglükeemiale pidevalt, toniseerivas režiimis ja hoolimata insuliini liigsest sekretsioonist ei normaliseeru glükeemia tase insuliiniresistentsuse taustal (joonis 7.8).
Hüperinsulinemia tagajärjeks on insuliiniretseptorite tundlikkuse ja arvu vähenemine, samuti supressioon.
retseptorijärgsed mehhanismid, mis vahendavad insuliini toimet (insuliiniresistentsus). Peamise glükoosi transporteri sisaldus lihas- ja rasvarakkudes (GLUT-4) väheneb vistseraalse rasvumisega inimestel 40% ja DM-2-ga inimestel 80%. Hepatotsüütide insuliiniresistentsuse ja portaalhüperinsulineemia tõttu glükoosi hüperproduktsioon maksas, ja tekib tühja kõhuga hüperglükeemia, mis tuvastatakse enamikul DM-2-ga patsientidel, sealhulgas haiguse varases staadiumis.
Hüperglükeemia iseenesest mõjutab negatiivselt β-rakkude sekretoorse aktiivsuse olemust ja taset (glükoosi toksilisus). Pikaajaline, paljude aastate ja aastakümnete jooksul, olemasolev hüperglükeemia viib lõpuks insuliinitootmise vähenemiseni β-rakkude poolt ja patsiendil võivad tekkida mõned sümptomid. insuliinipuudus- kehakaalu langus, ketoos koos kaasnevate nakkushaigustega. Insuliini jääkproduktsioon, mis on piisav ketoatsidoosi vältimiseks, säilib aga DM-2-s peaaegu alati.
Epidemioloogia
CD-2 määrab diabeedi epidemioloogia üldiselt, kuna see moodustab umbes 98% selle haiguse juhtudest. CD-2 levimus on erinevates riikides ja etnilistes rühmades erinev. Euroopa keeles
 Riis. 7.8.β-rakkude sekretoorne düsfunktsioon II tüüpi suhkurtõve korral (1 kiire faas insuliini sekretsioon)
Riis. 7.8.β-rakkude sekretoorne düsfunktsioon II tüüpi suhkurtõve korral (1 kiire faas insuliini sekretsioon)
riigid, USA ja Venemaa Föderatsioon see moodustab umbes 5-6% elanikkonnast. Vanusega suureneb DM-2 esinemissagedus: täiskasvanute seas on DM-2 levimus 10%, üle 65-aastaste seas ulatub see 20% -ni. CD-2 esinemissagedus on Ameerika ja Hawaii saarte põliselanike seas 2,5 korda kõrgem; Pima hõimu (Arizonas) indiaanlaste seas ulatub see 50% -ni. hulgas maaelanikkond Indias, Hiinas, Tšiilis ja Aafrika riikides, kus on traditsiooniline elustiil, on CD-2 levimus väga madal (alla 1%). Teisest küljest ulatub see lääne tööstusriikidesse sisserändajate hulgas märkimisväärsele tasemele. Nii et Indiast ja Hiinast pärit immigrantide seas, kes elavad USA-s ja Suurbritannias, ulatub CD-2 levimus 12-15% -ni.
WHO prognoosib, et järgmise 20 aasta jooksul suureneb diabeetikute arv maailmas 122% (135 miljonilt 300 miljonile). Selle põhjuseks on nii rahvastiku progresseeruv vananemine kui ka linnastunud elustiili levik ja süvenemine. IN viimased aastad toimub CD-2 märkimisväärne "noorendamine" ja selle esinemissageduse tõus laste seas.
Kliinilised ilmingud
Enamikel juhtudel, puuduvad väljendunud kliinilised ilmingud, ja diagnoos tehakse rutiinse glükeemilise testiga. Haigus avaldub tavaliselt üle 40 aasta vanuselt, samas kui valdaval enamusel patsientidest on ülekaalulisus ja muud metaboolse sündroomi komponendid (vt lõik 11.2). Patsiendid ei kaeba töövõime languse üle, kui selleks pole muid põhjusi. Janu ja polüuuria kaebused saavutavad harva märkimisväärse raskusastme. Üsna sageli tunnevad patsiendid muret naha ja tupe sügeluse pärast ning seetõttu pöörduvad nad dermatoloogide ja günekoloogide poole. Kuna CD-2 tegelikust avaldumisest diagnoosimiseni möödub sageli aastaid (keskmiselt umbes 7 aastat), domineerib paljudel patsientidel haiguse avastamise ajal kliinilises pildis diabeedi hiliste tüsistuste sümptomid ja ilmingud. Pealegi toimub CD-2-ga patsiendi esimene visiit arstiabi saamiseks väga sageli hiliste tüsistuste tõttu. Seega saab patsiente haiglasse paigutada kirurgilistesse haiglatesse haavandiline kahjustus jalad (diabeetilise jala sündroom) pöörduge silmaarsti poole seoses nägemise järkjärgulise halvenemisega (diabeetiline retinopaatia), haiglasse sattuda südameatakkide, insultidega
jalgade veresoonte hävitava kahjustusega asutustes, kus neil avastatakse esmakordselt hüperglükeemia.
Diagnostika
Kõigi diabeeditüüpide jaoks ühised diagnostilised kriteeriumid on esitatud punktis 7.3. DM-2 diagnoos põhineb enamikul juhtudest hüperglükeemia tuvastamisel inimestel, kellel on DM-2 tüüpilised kliinilised tunnused (rasvumine, vanus üle 40–45 aasta, DM-2 positiivne perekonna ajalugu, muud komponendid). metaboolne sündroom), kliiniliste ja laboratoorsete tunnuste puudumisel insuliini absoluutne defitsiit (ilmne kaalulangus, ketoos). Kombinatsioon DM-2 kõrgest levimusest, selle loomupärasest pikast asümptomaatilisest kulgemisest ja võimalusest vältida selle raskeid tüsistusi selles seisundis varajane diagnoosimine vajaduse ette kindlaks määrata sõelumine, need. küsitluse läbiviimine CD-2 välistamiseks inimeste seas, kellel puuduvad haiguse sümptomid. Peamine test, nagu mainitud, on otsustavus tühja kõhu glükeemiline tase. Seda näidatakse järgmistes olukordades:
1. Kõigil üle 45-aastastel inimestel, eriti ülekaalulistel inimestel (KMI üle 25 kg / m 2), intervalliga üks kord 3 aasta jooksul.
2. Rohkem noor vanus liigse kehakaalu (KMI üle 25 kg / m2) ja täiendavate riskitegurite, sealhulgas:
Istuv eluviis;
CD-2 lähisugulastel;
Kuulumine rahvustesse, kellel on kõrge risk haigestuda CD-2-sse (afroameeriklased, hispaanlased, põlisameeriklased jne);
Naised, kes on sünnitanud lapse kaaluga üle 4 kg ja/või kellel on anamneesis rasedusdiabeet;
Arteriaalne hüpertensioon (≥ 140/90 mm Hg);
HDL > 0,9 mmol/l ja/või triglütseriidid > 2,8 mmol/l;
polütsüstiliste munasarjade sündroom;
NTG ja NGNT;
Südame-veresoonkonna haigused.
DM-2 esinemissageduse märkimisväärne suurenemine laste seas tingib vajaduse glükeemia taseme määramiseks skriininguga. laste ja teismeliste seas(alates 10-aastaselt 2-aastase intervalliga või algusega
puberteet, kui see toimus varasemas eas), kuuluvad kõrge riskiga rühmadesse, mille hulka kuuluvad lapsed ülekaaluline(KMI ja/või kaal > 85 protsentiil vanuse järgi või kaal üle 120% ideaalkaalust) ja mis tahes kaks järgmist täiendavat riskitegurit:
CD-2 esimese või teise sugulusliini sugulaste seas;
Kuulumine kõrge riskiga rahvusesse;
Insuliiniresistentsusega seotud kliinilised ilmingud (acanthosis nigricans, arteriaalne hüpertensioon, düslipideemia);
Diabeet, sealhulgas rasedusaegne, emal.
Diferentsiaaldiagnoos
Suurima kliinilise tähtsusega on CD-2 ja CD-1 diferentsiaaldiagnostika, mille põhimõtteid on kirjeldatud punktis 7.5 (tabel 7.6). Nagu mainitud, põhineb see enamikul juhtudel kliinilise pildi andmetel. Juhtudel, kui diabeedi tüüpi on raske kindlaks teha või kahtlustatakse mõnda harvaesinevat diabeedivarianti, sh pärilike sündroomide korral, on kõige olulisem praktiline vastus, kas patsient vajab insuliinravi.
Ravi
DM-2 ravi põhikomponendid on: dieetteraapia, kehalise aktiivsuse suurendamine, hüpoglükeemiline ravi, DM-i hiliste tüsistuste ennetamine ja ravi. Kuna enamik DM-2-ga patsiente on rasvunud, peaks dieet olema suunatud kehakaalu langetamisele (hüpokaloorne) ja hiliste tüsistuste, eelkõige makroangiopaatia (ateroskleroosi) ennetamisele. hüpokaloriline dieet vajalik kõigile liigse kehakaaluga (KMI 25-29 kg/m2) või rasvunud (KMI> 30 kg/m2) patsientidele. Enamasti tuleks soovitada vähendada päevast toidu kaloraaži naistel 1000-1200 kcal-ni ja meestel 1200-1600 kcal-ni. Toidu põhikomponentide soovitatav suhe DM-2 puhul on sarnane DM-1 omaga (süsivesikud - 65%, valgud 10-35%, rasvad kuni 25-35%). Kasuta alkohol tuleks piirata, kuna see on oluline lisakalorite allikas, lisaks alkoholi tarbimine ravi taustal
PII koos sulfonüüluurea ravimite ja insuliiniga võib esile kutsuda hüpoglükeemia tekke (vt lõik 7.7.3).
Soovitused jaoks laienemine kehaline aktiivsus peab olema individualiseeritud. Alguses on soovitatav mõõduka intensiivsusega aeroobne treening (kõndimine, ujumine) 30-45 minutit 3-5 korda päevas (umbes 150 minutit nädalas). Tulevikus on vajalik kehalise aktiivsuse järkjärguline suurendamine, mis aitab oluliselt kaasa kehakaalu vähenemisele ja normaliseerumisele. Lisaks aitab füüsiline aktiivsus vähendada insuliiniresistentsust ja omab hüpoglükeemilist toimet. Dieetteraapia ja suurenenud kehalise aktiivsuse kombinatsioon ilma hüpoglükeemilisi ravimeid välja kirjutamata võimaldab säilitada DM-i kompensatsiooni vastavalt seatud eesmärkidele (tabel 7.3) ligikaudu 5% DM-2-ga patsientidest.
Ettevalmistused selleks hüpoglükeemiline ravi CD-2-ga võib jagada nelja põhirühma.
I. Ravimid, mis aitavad vähendada insuliiniresistentsust (sensibilisaatorid). Sellesse rühma kuuluvad metformiin ja tiasolidiindioonid. Metformiin on ainus praegu kasutatav ravim selles rühmas biguaniidid. Selle toimemehhanismi peamised komponendid on järgmised:
1. Maksa glükoneogeneesi pärssimine (maksa glükoosi tootmise vähenemine), mis viib tühja kõhu glükeemia vähenemiseni.
2. Insuliiniresistentsuse vähenemine (perifeersete kudede, peamiselt lihaste suurenenud glükoosi kasutamine).
3. Anaeroobse glükolüüsi aktiveerimine ja glükoosi imendumise vähendamine peensooles.
Metformiin on hüpoglükeemilise ravi esmavaliku ravim II tüüpi diabeedi, rasvumise ja tühja kõhuga hüperglükeemiaga patsientidel. Algannus on 500 mg öösel või õhtusöögi ajal. Edaspidi suureneb annus järk-järgult 2-3 grammi 2-3 annuseks. Kõrvaltoimetest on suhteliselt sagedased düspeptilised sümptomid (kõhulahtisus), mis on tavaliselt mööduvad ja kaovad iseenesest 1-2 nädala pärast ravimi võtmist. Kuna metformiinil ei ole insuliini tootmist stimuleerivat toimet, ei esine selle ravimi monoteraapia ajal hüpoglükeemiat.
areneda (selle toimet nimetatakse antihüperglükeemiliseks, mitte hüpoglükeemiliseks). Metformiini määramise vastunäidustused on rasedus, raske südame-, maksa-, neeru- ja muude elundite puudulikkus, samuti muu päritoluga hüpoksilised seisundid. Üliharvaesinev tüsistus, mis tekib metformiini väljakirjutamisel ilma ülaltoodud vastunäidustusi arvesse võtmata, on laktatsidoos, mis on anaeroobse glükolüüsi hüperaktivatsiooni tagajärg.
Tiasolidiindioonid(pioglitasoon, rosiglitasoon) on peroksisoomi proliferaatoriga aktiveeritud retseptori agonistid (PPAR-γ). Tiasolidiindioonid aktiveerivad glükoosi ja lipiidide metabolismi lihas- ja rasvkoes, mis toob kaasa endogeense insuliini aktiivsuse tõusu, s.o. Insuliiniresistentsuse kõrvaldamiseks (insuliini sensibilisaatorid). Pioglitasooni päevane annus on 15-30 mg / päevas, rosiglitasooni - 4-8 mg (1-2 annuse jaoks). Tiasolidiindioonide kombinatsioon metformiiniga on väga tõhus. Tiasolidiindioonide määramise vastunäidustuseks on maksa transaminaaside taseme tõus (2,5 korda või rohkem). Lisaks hepatotoksilisusele on tiasolidiindioonide kõrvaltoimeteks vedelikupeetus ja tursed, mis on sagedasemad, kui neid kombineerida insuliiniga.
II. Ravimid, mis toimivadβ rakke ja suurendab insuliini sekretsiooni. Sellesse rühma kuuluvad sulfonüüluurea ravimid ja gliniidid (prandiaalsed glükeemilised regulaatorid), mida kasutatakse peamiselt glükeemilise taseme normaliseerimiseks pärast sööki. peamine sihtmärk sulfonüüluurea ravimid(PSM) on pankrease saarekeste β-rakud. PSM-id seonduvad β-rakumembraani spetsiifiliste retseptoritega. See viib ATP-st sõltuvate kaaliumikanalite sulgumiseni ja rakumembraani depolariseerumiseni, mis omakorda aitab kaasa rakumembraani avanemisele. kaltsiumi kanalid. Kaltsiumi sisenemine β-rakkudesse põhjustab nende degranulatsiooni ja insuliini vabanemist verre. Kliinilises praktikas kasutatakse palju PSM-i, mis erinevad hüpoglükeemilise toime kestuse ja raskusastme poolest (tabel 7.9).
Tab. 7.9. Sulfonüüluuread
 PSM-i peamine ja üsna sage kõrvalnäht on hüpoglükeemia (vt lõik 7.7.3). See võib tekkida ravimi üleannustamise, selle kumulatsiooni (neerupuudulikkuse) korral,
PSM-i peamine ja üsna sage kõrvalnäht on hüpoglükeemia (vt lõik 7.7.3). See võib tekkida ravimi üleannustamise, selle kumulatsiooni (neerupuudulikkuse) korral,
dieedi (söögikordade vahelejätmine, alkoholi joomine) või režiimi (oluline füüsiline aktiivsus, enne mida ei vähendata PSM-i annust ega tarbita süsivesikuid) mittejärgimine.
Rühma juurde gliniidid(prandiaalsed glükeemilised regulaatorid) on repagliniid(bensoehappe derivaat; päevane annus 0,5-16 mg/päevas) ja nategliniid(D-fenüülalaniini derivaat; päevane annus 180-540 mg/päevas). Pärast manustamist interakteeruvad ravimid kiiresti ja pöörduvalt β-raku sulfonüüluurea retseptoriga, mille tulemuseks on insuliinitaseme lühiajaline tõus, mis jäljendab normaalselt selle sekretsiooni esimest faasi. Ravimeid võetakse 10-20 minutit enne põhitoidukordi, tavaliselt 3 korda päevas.
III. Ravimid, mis vähendavad glükoosi imendumist soolestikus.
Sellesse rühma kuuluvad akarboos ja guarkummi. Akarboosi toimemehhanism on α-glükosidaaside pöörduv blokaad peensoolde, mille tulemusena aeglustuvad süsivesikute järjestikuse fermentatsiooni ja imendumise protsessid, väheneb glükoosi resorptsiooni ja maksa sisenemise kiirus ning söögijärgse glükeemia tase. Akarboosi algannus on 50 mg 3 korda päevas, edaspidi võib annust suurendada 100 mg-ni 3 korda päevas; ravimit võetakse vahetult enne sööki või söögi ajal. Akarboosi peamine kõrvalmõju on soole düspepsia (kõhulahtisus, kõhupuhitus), mis on seotud imendumata süsivesikute sattumisega jämesoolde. Akarboosi hüpoglükeemiline toime on väga mõõdukas (tabel 7.10).
Kliinilises praktikas kombineeritakse hüpoglükeemilisi tablette tõhusalt üksteisega ja insuliinipreparaatidega, kuna enamikul patsientidest on samaaegselt nii tühja kõhuga kui ka söögijärgne hüperglükeemia. Neid on arvukalt fikseeritud kombinatsioonid ravimid ühes tabletis. Kõige sagedamini kombineeritakse metformiini ühes tabletis erinevate PSM-idega, samuti metformiini tiasolidiindioonidega.
Tab. 7.10. Tablettide hüpoglükeemiliste ravimite toimemehhanism ja potentsiaalne efektiivsus
 IV. Insuliinid ja insuliini analoogid
IV. Insuliinid ja insuliini analoogid
Teatud etapis hakkab insuliinipreparaate saama kuni 30–40% II tüüpi diabeediga patsientidest. DM-2 insuliinravi näidustused on toodud lõigu 7.4 alguses. Kõige tavalisem variant II tüüpi diabeediga patsientidele insuliinravile üleminekuks on pika toimeajaga insuliini (NPH-insuliin, glargiin või detemiir) väljakirjutamine koos manustatavate hüpoglükeemiliste tablettidega. Olukorras, kus tühja kõhu glükeemia taset ei ole võimalik metformiini määramisega kontrollida või viimane on vastunäidustatud, määratakse patsiendile õhtune (öine) insuliinisüst. Kui tabletipreparaatide abil ei ole võimalik nii tühja kõhuga kui ka söögijärgset glükeemiat kontrollida, viiakse patsient üle monoinsuliinravile. Tavaliselt toimub DM-2-ga insuliinravi nn "traditsiooniline" skeem mis hõlmab pika- ja lühitoimelise insuliini fikseeritud annuste määramist. Selles plaanis
mugavad standardsed insuliinisegud, mis sisaldavad ühes viaalis lühitoimelist (ülilühikest) ja pikatoimelist insuliini. Traditsioonilise insuliinravi valiku määrab asjaolu, et DM-2-ga määratakse see sageli eakatele patsientidele, kelle treenimine insuliini annust iseseisvalt muutma on keeruline. Lisaks suurendab hüpoglükeemia riski intensiivne insuliinravi, mille eesmärk on säilitada süsivesikute ainevahetuse kompenseerimine tasemel, mis läheneb normoglükeemilisele tasemele. Kui kerge hüpoglükeemia ei kujuta endast tõsist ohtu noortel patsientidel, siis vanematel patsientidel, kellel on vähenenud hüpoglükeemia lävi, võib see avaldada südame-veresoonkonna süsteemile väga kahjulikku mõju. Noortele II tüüpi diabeediga patsientidele, aga ka tõhusa õppimise võimaluse osas paljutõotavatele patsientidele võib määrata insuliinravi intensiivse versiooni.
Prognoos
DM-2-ga patsientide puude ja surma peamine põhjus on hilised tüsistused (vt lõik 7.8), kõige sagedamini diabeetiline makroangiopaatia. Individuaalsete hiliste tüsistuste tekkimise riski määrab tegurite kompleks, mida käsitletakse vastavates peatükkides. Nende arengu universaalne riskitegur on krooniline hüperglükeemia. Seega põhjustab 2. tüüpi diabeediga patsientide HbA1c taseme 1% langus üldise suremuse vähenemist vastavalt umbes 20%, 2% ja 3% - umbes 40%.
7.7. DIABEEDI Ägedad komplikatsioonid
7.7.1. diabeetiline ketoatsidoos
Diabeetiline ketoatsidoos (DKA)- DM-1 dekompensatsioon, mis on põhjustatud insuliini absoluutsest puudusest õigeaegse ravi puudumisel, mis lõpeb ketoatsidootilise koomaga (CK) ja surmaga.
Etioloogia
DKA põhjus on absoluutne insuliinipuudus. See või teine DKA raskusaste määratakse enamikul patsientidest DM-1 avaldumise ajal (10–20% kõigist DKA juhtudest).
I tüüpi diabeedi diagnoosiga patsiendil võib DKA tekkida siis, kui insuliini manustamine lõpetatakse, sageli patsiendi enda poolt (13% DKA juhtudest), kaasuvate haiguste, peamiselt nakkushaiguste taustal, ilma ravita. insuliini annuse suurendamine
Tab. 7.11. diabeetiline ketoatsidoos
 Kuni 20% DKA juhtudest noortel I tüüpi diabeediga patsientidel on seotud psühholoogiliste probleemide ja/või häiretega. söömiskäitumine(hirm kaalutõusu ees, hirm hüpoglükeemia ees, noorukite probleemid). Paljudes riikides on DKA üsna levinud põhjus
Kuni 20% DKA juhtudest noortel I tüüpi diabeediga patsientidel on seotud psühholoogiliste probleemide ja/või häiretega. söömiskäitumine(hirm kaalutõusu ees, hirm hüpoglükeemia ees, noorukite probleemid). Paljudes riikides on DKA üsna levinud põhjus
insuliini ärajätmine patsiendi enda poolt ravimite kõrge hinna tõttu mõne elanikkonnarühma jaoks (tabel 7.11).
Patogenees
DKA patogenees põhineb absoluutsel insuliinipuudusel koos kontrainsulaarsete hormoonide, näiteks glükagooni, katehhoolamiinide ja kortisooli tootmise suurenemisega. Selle tulemusena suureneb märkimisväärselt maksa glükoosi tootmine ja perifeersete kudede selle kasutamise rikkumine, hüperglükeemia suurenemine ja rakuvälise ruumi osmolaarsuse rikkumine. Insuliinipuudus kombinatsioonis kontrainsulaarsete hormoonide suhtelise liiaga DKA-s põhjustab vabade rasvhapete vabanemist vereringesse (lipolüüs) ja nende ohjeldamatut oksüdeerumist maksas ketoonkehadeks (β-hüdroksübutüraat, atsetoatsetaat, atsetoon), mille tulemuseks on hüperketoneemia. ja edasine metaboolne atsidoos. Raske glükosuuria tagajärjel areneb osmootne diurees, dehüdratsioon, naatriumi, kaaliumi ja teiste elektrolüütide kadu (joon. 7.9).
Epidemioloogia
Uute DKA juhtude sagedus on 5–8 1000 DM-1-ga patsiendi kohta aastas ja see sõltub otseselt DM-ga patsientide arstiabi korralduse tasemest. Ameerika Ühendriikides toimub igal aastal ligikaudu 100 000 haiglaravi DKA tõttu ja arvestades iga patsiendi haiglaravi maksumust 13 000 dollarit aastas. haiglaravi DKA kulutab üle 1 miljardi dollari aastas. Vene Föderatsioonis registreeriti 2005. aastal DKA 4,31% lastest, 4,75% noorukitest ja 0,33% täiskasvanud DM-1-ga patsientidest.
Kliinilised ilmingud
DKA areng võib olenevalt selle põhjustanud põhjusest kesta mitu nädalat kuni päevani. Enamikul juhtudel eelnevad DKA-le dekompenseeritud diabeedi sümptomid, kuid mõnikord ei pruugi neil olla aega areneda. DKA kliinilisteks sümptomiteks on polüuuria, polüdipsia, kaalulangus, üldine kõhuvalu ("diabeetiline pseudoperitoniit"), dehüdratsioon, tugev nõrkus, atsetoonilõhn (või puuviljalõhn) ja teadvuse järkjärguline hägustumine. Tõeline kooma DKA-s on varajase diagnoosimise tõttu viimasel ajal suhteliselt harva arenenud. Füüsilisel läbivaatusel ilmnevad dehüdratsiooni tunnused: vähenenud
 Riis. 7.9. Ketoatsidootilise kooma patogenees
Riis. 7.9. Ketoatsidootilise kooma patogenees
naha turgor ja silmamuna tihedus, tahhükardia, hüpotensioon. Kaugelearenenud juhtudel areneb Kussmauli hingamine. Rohkem kui 25%-l DKA-ga patsientidest tekib oksendamine, mis võib oma värvilt meenutada kohvipaksu.
Diagnostika
See põhineb kliinilise pildi andmetel, CD-1 esinemise näidustustel patsiendil ja laboratoorsetel andmetel. DKA-le on iseloomulik hüperglükeemia (mõnel juhul ebaoluline), ketonuuria, metaboolne atsidoos, hüperosmolaarsus (tabel 7.12).
Tab. 7.12. Diabeedi ägedate tüsistuste laboridiagnoos
 Diabeedi ägeda dekompensatsiooniga patsientide uurimisel on vaja määrata glükeemia, kreatiniini ja uurea, elektrolüütide tase, mille põhjal arvutatakse efektiivne osmolaarsus. Lisaks on vajalik happe-aluse oleku hindamine. Efektiivne osmolaarsus(EO) arvutatakse järgmise valemi abil: 2 *. Tavaline EO on 285–295 mOsm / l.
Diabeedi ägeda dekompensatsiooniga patsientide uurimisel on vaja määrata glükeemia, kreatiniini ja uurea, elektrolüütide tase, mille põhjal arvutatakse efektiivne osmolaarsus. Lisaks on vajalik happe-aluse oleku hindamine. Efektiivne osmolaarsus(EO) arvutatakse järgmise valemi abil: 2 *. Tavaline EO on 285–295 mOsm / l.
Enamikul DKA-ga patsientidel on leukotsütoos, mille raskusaste on võrdeline ketoonkehade tasemega veres. Tase naatrium, reeglina väheneb see vedeliku osmootse väljavoolu tõttu intratsellulaarsetest ruumidest rakuvälistesse ruumidesse vastusena hüperglükeemiale. Harva võib naatriumisisaldus olla valepositiivne raske hüper-
triglütserideemia. Tase kaalium Seerum võib algselt olla kõrgendatud, kuna see liigub rakuvälistest ruumidest.
Diferentsiaaldiagnoos
Muud diabeediga patsientide teadvusekaotuse põhjused. Hüperosmolaarse koomaga diferentsiaaldiagnostika ei tekita reeglina raskusi (see areneb eakatel II tüüpi diabeediga patsientidel) ega oma suurt kliinilist tähtsust, sest Mõlema haigusseisundi ravi põhimõtted on sarnased. Kui diabeediga patsiendi teadvuse kaotuse põhjust ei ole võimalik kiiresti välja selgitada, näidatakse talle glükoosi sisseviimist, kuna. hüpoglükeemilised seisundid on palju tavalisemad ja kiire positiivne dünaamika glükoosi manustamise taustal võimaldab iseenesest välja selgitada teadvuse kaotuse põhjuse.
Ravi
DKA ravi hõlmab rehüdratatsiooni, hüperglükeemia korrigeerimist, elektrolüütide häireid ja diabeedi dekompensatsiooni põhjustanud haiguste ravi. Ravi viiakse kõige optimaalsemalt läbi spetsialiseeritud meditsiiniasutuse intensiivravi osakonnas. Raske kaasuva südamepatoloogiata täiskasvanud patsientidel juba haiglaeelses staadiumis esmase meetmena rehüdratsioon isotoonilist lahust (0,9% NaCl) soovitatakse manustada ligikaudu liiter tunnis (umbes 15-20 ml kehakaalu kilogrammi kohta tunnis). Vedelikupuuduse täielik asendamine, mis DKA puhul on 100-200 ml 1 kg kehakaalu kohta, tuleb saavutada esimesel ravipäeval. Samaaegse südame- või neerupuudulikkuse korral tuleks seda ajavahemikku pikendada. Lastele on rehüdratsioonravi isotoonilise lahuse soovitatav kogus 10-20 ml 1 kg kehakaalu kohta tunnis, kusjuures esimese 4 tunni jooksul ei tohiks see ületada 50 ml 1 kg kehakaalu kohta. Täielik rehüdratsioon on soovitatav saavutada umbes 48 tunni jooksul. Pärast seda, kui glükeemia tase langeb paralleelse insuliinravi taustal ligikaudu 14 mmol / l-ni, lülituvad nad üle 10% glükoosilahuse transfusioonile, mis jätkab rehüdratsiooni.
Nüüd on vastu võetud mõiste "väikesed annused". insuliini DKA ravis. Kasutatakse ainult lühitoimelist insuliini. Intravenoosse insuliini kõige optimaalsem kasutamine
rida. Intramuskulaarne insuliini manustamine, mis on vähem efektiivne, on võimalik ainult DKA mõõduka raskusega, stabiilse hemodünaamika korral ja kui intravenoosne ravi ei ole võimalik. Viimasel juhul tehakse süstid kõhu sirglihasesse, samal ajal kui insuliinisüstlale asetatakse nõel. intramuskulaarsed süstid(usaldusväärseks intramuskulaarseks süstimiseks) ja selle nõela kaudu tõmmatakse viaalist süstlasse insuliin.
Insuliini intravenoosseks manustamiseks on mitu võimalust. Esiteks saab insuliini süstida infusioonisüsteemi "igemesse", samal ajal kui vajalik kogus insuliini tõmmatakse insuliinisüstlasse, mille järel tõmmatakse sellesse 1 ml isotoonilist lahust. Kuni glükeemia tase jõuab 14 mmol / l-ni, süstitakse patsiendile iga tunni järel 6-10 ühikut lühitoimelist insuliini; edasi (paralleelselt rehüdratatsioonilahuse muutmisega isotooniliselt 10% glükoosile) sõltuvalt tunnis määratud glükeemia näitajatest vähendatakse insuliini annust 4-8 ühikuni tunnis. Soovitatav glükeemilise taseme languse kiirus ei tohi ületada 5 mmol/l tunnis. Veel üks intravenoosse insuliinravi võimalus hõlmab perfuusori kasutamist. Perfuusori lahuse valmistamiseks võetakse järgmine suhe: 50 ühikule lühitoimelisele insuliinile lisatakse 2 ml 20% inimese albumiini lahust, misjärel lisatakse 50 mg 0,9% isotoonilist lahust. Kui valitakse insuliini intramuskulaarne manustamisviis, manustatakse esialgu 20 ühikut lühitoimelist insuliini, seejärel 6 ühikut iga tund ja pärast glükeemia taseme 14 mmol/l saavutamist vähendatakse annust 4 ühikuni tunnis. Pärast hemodünaamika täielikku stabiliseerumist ja happe-aluse häirete kompenseerimist viiakse patsient üle subkutaansetele insuliinisüstidele.
Nagu märgitud, hoolimata märkimisväärsest kaaliumipuudus kehas (kogukaotus 3-6 mmol / kg), DKA-ga võib selle tase enne insuliinravi algust veidi tõusta. Siiski on soovitatav alustada kaaliumkloriidi lahuse transfusiooni samaaegselt insuliinravi alustamisega, kui plasma kaaliumisisaldus on alla 5,5 mmol/L. Kaaliumipuuduse edukas korrigeerimine toimub ainult pH normaliseerumise taustal. Madala pH korral väheneb oluliselt kaaliumi sissevõtt rakku, sellega seoses on võimalusel soovitav ülekantud kaaliumkloriidi doos kohandada konkreetse pH indikaatoriga (tabel 7.13).
Tab. 7.13. Kaaliumipuuduse korrigeerimise skeem
 * Arvutamiseks kasutatakse järgmisi andmeid:
* Arvutamiseks kasutatakse järgmisi andmeid:
1 g KCl = 13,4 mmol; 1 mmol KCl = 0,075 g KC1 4% lahuses: 100 ml-s - 4 g KC1, 25 ml-s - 1 g KC1, 10 ml-s 0,4 g KC1.
Diabeedi dekompensatsiooni põhjuseks on sageli nakkushaigused(püelonefriit, nakatunud haavand diabeetilise jala sündroomi korral, kopsupõletik, sinusiit jne). Kehtib reegel, mille kohaselt DKA-s on antibiootikumravi ette nähtud peaaegu kõigile madala palavikuga või palavikuga patsientidele, isegi kui infektsioonikolde pole nähtav, kuna kehatemperatuuri tõus ei ole DKA-le endale tüüpiline. .
Prognoos
Suremus DKA-sse on 0,5–5%, kusjuures enamik juhtudest on tingitud hilisest ja oskusteta arstiabist. Suremus on kõrgeim (kuni 50%) eakate patsientide seas.
7.7.2. Hüperosmolaarne kooma
Hüperosmolaarne kooma(GOK) on haruldane DM-2 äge tüsistus, mis areneb tõsise dehüdratsiooni ja hüperglükeemia tagajärjel absoluutse insuliinipuuduse puudumisel, millega kaasneb kõrge suremus (tabel 7.14).
Etioloogia
GOK areneb reeglina II tüüpi diabeediga eakatel patsientidel. Sellised patsiendid on enamasti üksildased, elavad ilma hoolitsuseta, eiravad oma seisundit ja enesekontrolli ning ei võta piisavalt vedelikku. Infektsioonid põhjustavad sageli dekompensatsiooni (diabeetilise jala sündroom, kopsupõletik, äge püelonefriit), ajuhäireid.
vereringe- ja muud seisundid, mille tõttu patsiendid liiguvad halvasti, ei võta hüpoglükeemilisi ravimeid ja vedelikke.
Tab. 7.14. Hüperosmolaarne kooma (GOC)
 Patogenees
Patogenees
Suurenev hüperglükeemia ja osmootne diurees põhjustavad tõsist dehüdratsiooni, mida ülaltoodud põhjustel väljastpoolt ei täiendata. Hüperglükeemia ja dehüdratsiooni tagajärjeks on plasma hüperosmolaarsus. GOC patogeneesi lahutamatuks komponendiks on suhteline insuliini defitsiit ja kontra-insuliini hormoonide liig, kuid DM-2-sse jääv insuliini jääksekretsioon on piisav lipolüüsi ja ketogeneesi pärssimiseks, mille tulemusena areneb areng. ketoatsidoosi ei esine.
Mõnel juhul võib kudede hüpoperfusiooni taustal määrata hüperlaktateemia tagajärjel mõõduka atsidoosi. Raske hüperglükeemia korral suureneb tserebrospinaalvedeliku osmootse tasakaalu säilitamiseks rakkudest tuleva naatriumi sisaldus. aju kus vahetatakse kaaliumi. Närvirakkude transmembraanne potentsiaal on häiritud. Teadvuse progresseeruv hägustumine areneb koos konvulsiivse sündroomiga (joonis 7.10).
Epidemioloogia
GOC moodustab 10–30% ägedatest hüperglükeemilistest seisunditest II tüüpi diabeediga täiskasvanud ja eakatel patsientidel. Ligikaudu 2/3 GOK juhtudest areneb inimestel, kellel on varem diagnoosimata diabeet.
Kliinilised ilmingud
Hüperosmolaarse kooma kliinilise pildi tunnused on järgmised:
Dehüdratsiooni ja hüpoperfusiooni nähtude ja tüsistuste kompleks: janu, limaskestade kuivus, tahhükardia, arteriaalne hüpotensioon, iiveldus, nõrkus, šokk;
fokaalsed ja generaliseerunud krambid;
Palavik, iiveldus ja oksendamine (40-65% juhtudest);
Kaasuvatest haigustest ja tüsistustest on levinud süvaveenide tromboos, kopsupõletik, tserebrovaskulaarsed häired ja gastroparees.
Diagnostika
See põhineb kliinilise pildi, patsiendi vanuse ja CD-2 anamneesi andmetel, raske hüperglükeemia ketonuuria puudumisel ja ketoatsidoos. GOK tüüpilised laboratoorsed tunnused on esitatud tabelis. 7.12.
 Riis. 7 .10.
Hüperosmolaarse kooma patogenees
Riis. 7 .10.
Hüperosmolaarse kooma patogenees
Diferentsiaaldiagnoos
muud ägedad seisundid areneb DM-ga patsientidel, kõige sagedamini kaasuva patoloogiaga, mis viis DM-i raske dekompensatsioonini.
Ravi
GOC ravi ja jälgimine, välja arvatud mõned tunnused, ei erine ketoatsidootilise diabeetilise kooma puhul kirjeldatust (jaotis 7.7.1):
Suurem esialgse rehüdratsiooni maht 1,5-2 liitrit 1 tunni kohta; 1 l - 2. ja 3. tunniks, seejärel 500 ml / h isotoonilist naatriumkloriidi lahust;
Kaaliumi sisaldavate lahuste sisseviimise vajadus on reeglina suurem kui ketoatsidootilise kooma korral;
Insuliinravi on sarnane QC-ga, kuid insuliinivajadus on väiksem ja glükeemia taset tuleb vähendada mitte kiiremini kui 5 mmol / l tunnis, et vältida ajuturse teket;
Hüpotoonilise lahuse (NaCl 0,45%) sisseviimist on kõige parem vältida (ainult raske hüpernatreemia korral: > 155 mmol/l ja/või efektiivne osmolaarsus > 320 mOsm/l);
Bikarbonaati ei ole vaja manustada (ainult pH-ga atsidoosi eriintensiivravi osakonnas< 7,1).
Prognoos
Korea valitsuse suremus on kõrge ja ulatub 15–60% -ni. Halvim prognoos on eakatel patsientidel, kellel on raske kaasuv haigus, mis on sageli DM dekompensatsiooni ja GOC tekke põhjuseks.
7.7.3. hüpoglükeemia
hüpoglükeemia- Vere glükoosisisalduse langus<2,2- 2,8 ммоль/л), сопровождающее клинический синдром, характеризующийся признаками активации симпатической нервной системы и/или дисфункцией центральной нервной системы. Гипогликемия как лабораторный феномен не тождественен понятию «гипогликемическая симптоматика», поскольку лабораторные данные и клиническая картина не всегда совпадают.
Etioloogia
Insuliinipreparaatide ja selle analoogide, samuti sulfonüüluurea preparaatide üleannustamine;
ebapiisav toidutarbimine muutumatu hüpoglükeemilise ravi taustal;
Alkohoolsete jookide vastuvõtt;
Füüsiline aktiivsus muutumatu hüpoglükeemilise ravi taustal ja / või ilma täiendava süsivesikute tarbimiseta;
Diabeedi hiliste tüsistuste (autonoomne neuropaatia koos gastropareesiga, neerupuudulikkus) ja paljude teiste haiguste (neerupealiste puudulikkus, hüpotüreoidism, maksapuudulikkus, pahaloomulised kasvajad) tekkimine muutumatul hüpoglükeemilisel ravil (TSP jätkamine ja kumuleerimine neerupuudulikkuse taustal , säilitades insuliini sama annuse);
Insuliini manustamise tehnika rikkumine (subkutaanse asemel intramuskulaarne süstimine);
Kunstlik hüpoglükeemia (patsiendi teadlik hüpoglükeemiliste ravimite üleannustamine);
Orgaaniline hüperinsulinism – insulinoom (vt lõik 10.3).
Patogenees
Hüpoglükeemia patogenees seisneb tasakaalustamatuses glükoosi verre sisenemise, selle kasutamise, insuliini taseme ja kontrainsulaarsete hormoonide vahel. Tavaliselt on glükeemia tasemel vahemikus 4,2-4,7 mmol/l insuliini tootmine ja vabanemine β-rakkudest pärsitud. Glükeemia taseme langusega alla 3,9 mmol / l kaasneb kontrainsulaarsete hormoonide (glükagoon, kortisool, kasvuhormoon, adrenaliin) tootmise stimuleerimine. Neuroglükopeenilised sümptomid arenevad glükeemia taseme langusega alla 2,5-2,8 mmol / l. Üleannustamine insuliini ja/või ravimid sulfonüüluurea hüpoglükeemia areneb eksogeense või endogeense hormooni otsese hüpoglükeemilise toime tõttu. Sulfonüüluurea ravimite üleannustamise korral võivad hüpoglükeemilised sümptomid pärast rünnaku leevendamist korduda mitu korda, kuna mitmete ravimite toimeaeg võib ulatuda päevani või kauemaks. TSP-d, millel ei ole insuliini tootmist stimuleerivat toimet (metformiin, tiasolidiindioonid), ei saa iseenesest hüpoglükeemiat põhjustada, kuid kui neid lisada sulfonüüluurea ravimitele või insuliinile, võib viimaste sama annuse võtmine põhjustada hüpoglükeemiat hüpoglükeemilise aine kumuleerumise tõttu. kombineeritud ravi mõju (tabel .7.15).
Tab. 7.15. hüpoglükeemia
 Tabeli lõpp. 7.15
Tabeli lõpp. 7.15
 Kui saate alkohol maksas on glükoneogeneesi pärssimine, mis on kõige olulisem hüpoglükeemiat takistav tegur. Füüsiline treening aitavad kaasa insuliinist sõltumatule glükoosi kasutamisele, mille tõttu võivad nad muutumatu hüpoglükeemilise ravi taustal ja / või täiendava süsivesikute tarbimise puudumisel põhjustada hüpoglükeemiat.
Kui saate alkohol maksas on glükoneogeneesi pärssimine, mis on kõige olulisem hüpoglükeemiat takistav tegur. Füüsiline treening aitavad kaasa insuliinist sõltumatule glükoosi kasutamisele, mille tõttu võivad nad muutumatu hüpoglükeemilise ravi taustal ja / või täiendava süsivesikute tarbimise puudumisel põhjustada hüpoglükeemiat.
Epidemioloogia
Kerge, kiiresti pöörduv hüpoglükeemia I tüüpi diabeediga patsientidel, kes saavad intensiivset insuliinravi, võib tekkida mitu korda nädalas ja on suhteliselt kahjutu. Ühel intensiivset insuliinravi saavatel patsientidel esineb 1 raske hüpoglükeemia juhtum aastas. Enamikul juhtudel tekib hüpoglükeemia öösel. T2DM-i korral tekib 20% insuliini saavatest patsientidest ja 6% sulfonüüluurea ravimeid saavatest patsientidest 10 aasta jooksul vähemalt üks raske hüpoglükeemia episood.
Kliinilised ilmingud
On kaks peamist sümptomite rühma: adrenergilised, mis on seotud sümpaatilise närvisüsteemi aktiveerumisega ja adrenaliini vabanemisega neerupealiste poolt, ja neuroglükopeensed, mis on seotud kesknärvisüsteemi talitlushäiretega selle peamise närvisüsteemi puudulikkuse taustal. energia substraat. TO adrenergiline sümptomite hulka kuuluvad: tahhükardia, müdriaas; ärevus, agressiivsus; värisemine, külm higi, paresteesia; iiveldus, tugev nälg, hüpersalivatsioon; kõhulahtisus, liigne urineerimine. TO neuroglükopeenne sümptomite hulka kuuluvad asteenia,
vähenenud keskendumisvõime, peavalu, hirm, segasus, desorientatsioon, hallutsinatsioonid; kõne-, nägemis-, käitumishäired, amneesia, teadvusehäired, krambid, mööduv halvatus, kellele. Hüpoglükeemia süvenedes ei pruugi sümptomite raskuse ja järjestuse vahel olla selget seost. Esineda võivad ainult adrenergilised või ainult neuroglükopeenilised sümptomid. Mõnel juhul võivad patsiendid, vaatamata normoglükeemia taastumisele ja käimasolevale ravile, jääda stuporisse või isegi koomasse mitmeks tunniks või isegi päevaks. Pikaajaline hüpoglükeemia või selle sagedased episoodid võivad põhjustada kesknärvisüsteemis (eelkõige ajukoores) pöördumatuid muutusi, mille ilmingud varieeruvad märkimisväärselt deliristlikust ja hallutsinatoorsetest-paranoilistest episoodidest kuni tüüpiliste epilepsiahoogudeni, mille vältimatuks tagajärjeks on püsiv dementsus. .
Patsiendid taluvad subjektiivselt hüperglükeemiat kergemini kui isegi kerge hüpoglükeemia episoode. Seetõttu peavad paljud patsiendid hüpoglükeemia hirmu tõttu vajalikuks säilitada glükeemia suhteliselt kõrgel tasemel, mis tegelikult vastab haiguse dekompensatsioonile. Sellest stereotüübist üle saamine nõuab mõnikord arstide ja õppejõudude märkimisväärseid pingutusi.
Diagnostika
Hüpoglükeemia kliiniline pilt diabeediga patsiendil koos madala veresuhkru taseme laboratoorse (tavaliselt glükomeetri abil) tuvastamisega.
Diferentsiaaldiagnoos
Muud põhjused, mis põhjustavad teadvusekaotust. Kui diabeediga patsiendi teadvuse kaotuse põhjus pole teada ja glükeemia taseme kiiret analüüsi pole võimalik teha, näidatakse talle glükoosi sisseviimist. Sageli on vaja välja selgitada diabeediga patsientide sagedase hüpoglükeemia tekke põhjus. Enamasti on need tingitud ebapiisavast hüpoglükeemilisest ravist ja patsiendi vähesest teadmistest oma haiguse kohta. Tuleb meeles pidada, et mitmed haigused (neerupealiste puudulikkus, hüpotüreoidism, neeru- ja maksapuudulikkus), sealhulgas pahaloomulised kasvajad, võivad põhjustada hüpoglükeemilise ravi vajaduse vähenemist kuni selle täieliku tühistamiseni ("kadunud diabeet").
Ravi
Kerge hüpoglükeemia raviks, mille puhul patsient on teadvusel ja saab ennast aidata, piisab tavaliselt süsivesikuid sisaldava toidu või vedeliku võtmisest 1-2 leivaühikut (10-20 g glükoosi). See kogus sisaldub näiteks 200 ml magusas puuviljamahlas. Joogid on hüpoglükeemia peatamisel tõhusamad, kuna vedelal kujul imendub glükoos palju kiiremini. Kui sümptomid süvenevad vaatamata jätkuvale süsivesikute tarbimisele, on vaja intravenoosset glükoosi või intramuskulaarset glükagooni. Rasket hüpoglükeemiat koos teadvusekaotusega ravitakse sarnaselt. Sellisel juhul süstitakse patsiendile umbes 50 ml 40% glükoosilahus intravenoosselt. Glükoosi manustamist tuleb jätkata, kuni rünnak on leevendunud ja glükeemia normaliseerub, kuigi reeglina pole vaja suuremat annust - kuni 100 ml või rohkem. glükagoon manustada (tavaliselt tehases valmistatud täidetud süstlaga) intramuskulaarselt või subkutaanselt. Mõne minuti pärast normaliseerub glükagooni poolt glükogenolüüsi indutseerimisest tingitud glükeemia tase. Kuid see ei juhtu alati: kõrge insuliinisisaldusega veres on glükagoon ebaefektiivne. Glükagooni poolväärtusaeg on lühem kui insuliinil. Alkoholismi ja maksahaiguste korral on glükogeeni süntees häiritud ja glükagooni manustamine võib olla ebaefektiivne. Glükagooni manustamise kõrvalmõjuks võib olla oksendamine, mis tekitab aspiratsiooniohu. Soovitav on, et patsiendi sugulased valdaksid glükagooni süstimise tehnikat.
Prognoos
Kerge hüpoglükeemia hea haigushüvitisega koolitatud patsientidel on ohutu. Sage hüpoglükeemia on märk halvast DM-i kompensatsioonist; enamikul juhtudel on sellistel patsientidel rohkem või vähem väljendunud hüperglükeemia ja ülejäänud päeva jooksul kõrge glükeeritud hemoglobiini tase. Diabeedi hiliste tüsistustega eakatel patsientidel võib hüpoglükeemia esile kutsuda selliseid vaskulaarseid tüsistusi nagu müokardiinfarkt, insult, võrkkesta hemorraagia. Kuni 30 minutit kestev hüpoglükeemiline kooma piisava ravi ja kiire teadvuse naasmisega ei põhjusta reeglina tüsistusi ega tagajärgi.
7.8. DIABEEDI HILLISED TÜSISTUSED
Mõlemal DM-i tüübil tekivad hilised tüsistused. Kliiniliselt eristatakse viit peamist DM-i hilist tüsistust: makroangiopaatia, nefropaatia, retinopaatia, neuropaatia ja diabeetilise jala sündroom. Teatud tüüpi DM-i hiliste komplikatsioonide mittespetsiifilisuse määrab asjaolu, et nende peamine patogeneetiline seos on krooniline hüperglükeemia. Sellega seoses ei esine DM-1 ilmnemise ajal patsientidel peaaegu kunagi hilinenud tüsistusi, mis arenevad aastate ja aastakümnete jooksul, sõltuvalt ravi efektiivsusest. DM-1 puhul omandab reeglina suurim kliiniline tähtsus diabeetiline mikroangiopaatia(nefropaatia, retinopaatia) ja neuropaatia (diabeetilise jala sündroom). Vastupidi, DM-2 puhul avastatakse sageli hilised tüsistused juba diagnoosimise ajal. Esiteks on see tingitud asjaolust, et CD-2 avaldub juba ammu enne diagnoosi panemist. Teiseks on ateroskleroosil, mis kliiniliselt väljendub makroangiopaatias, palju DM-ga ühiseid patogeneesi seoseid. DM-2 puhul on suurim kliiniline tähtsus reeglina diabeetiline makroangiopaatia, mis diagnoosimise hetkel avastatakse valdaval enamusel patsientidest. Igal juhul varieerub üksikute hiliste komplikatsioonide kogum ja raskusaste nende paradoksaalsest täielikust puudumisest, hoolimata haiguse märkimisväärsest kestusest, kuni kõigi võimalike võimaluste kombinatsioonini raskes vormis.
Hilised komplikatsioonid on peamine surmapõhjus diabeeti põdevatel patsientidel ja võttes arvesse selle levimust - kõige olulisem meditsiiniline ja sotsiaalne terviseprobleem enamikus riikides. Selle tõttu ravi peamine eesmärk ja diabeediga patsientide jälgimine on selle hiliste tüsistuste ennetamine (esmane, sekundaarne, tertsiaarne).
7.8.1. Diabeetiline makroangiopaatia
Diabeetiline makroangiopaatia- kollektiivne kontseptsioon, mis ühendab suurte arterite aterosklerootilisi kahjustusi diabeedi korral,
kliiniliselt avaldub südame isheemiatõbi (CHD), ajuveresoonte, alajäsemete, siseorganite oblitereeriv ateroskleroos ja arteriaalne hüpertensioon (tabel 7.16).
Tab. 7.16. Diabeetiline makroangiopaatia
 Etioloogia ja patogenees
Etioloogia ja patogenees
Tõenäoliselt sarnane ateroskleroosi etioloogia ja patogeneesiga inimestel, kellel ei ole DM-i. Aterosklerootilised naastud ei erine mikroskoopilise struktuuri poolest inimestel, kellel on ja ilma DM. DM-i puhul võivad aga esile kerkida täiendavad riskifaktorid või DM süvendab teadaolevaid mittespetsiifilisi tegureid. Need, kellel on SD, peaksid sisaldama:
1. Hüperglükeemia. See on ateroskleroosi arengu riskitegur. HbA1c taseme tõus 1% võrra DM-2-ga patsientidel suureneb
Müokardiinfarkti tekkerisk on 15%. Hüperglükeemia aterogeense toime mehhanism ei ole täiesti selge, see võib olla seotud LDL-i metabolismi lõpp-produktide ja veresoonte seina kollageeni glükosüülimisega.
2. arteriaalne hüpertensioon(AG). Patogeneesis omistatakse suurt tähtsust neerukomponendile (diabeetiline nefropaatia). DM-2 hüpertensioon ei ole vähem oluline südameataki ja insuldi riskitegur kui hüperglükeemia.
3. Düslipideemia. Hüperinsulineemia, mis on T2DM-i insuliiniresistentsuse lahutamatu komponent, põhjustab HDL taseme langust, triglütseriidide tõusu ja tiheduse vähenemist, s.o. LDL suurenenud aterogeensus.
4. ülekaalulisus, mis mõjutab enamikku CD-2-ga patsiente, on sõltumatu ateroskleroosi, müokardiinfarkti ja insuldi riskifaktor (vt lõik 11.2).
5. insuliiniresistentsus. Hüperinsulineemia ja insuliini-proinsuliinitaoliste molekulide kõrge tase suurendavad ateroskleroosi riski, mis võib olla seotud endoteeli düsfunktsiooniga.
6. Vere hüübimise rikkumine. Diabeedi korral määratakse fibrinogeeni, trombotsüütide inhibiitori aktivaatori ja von Willebrandi faktori taseme tõus, mille tulemusena moodustub vere hüübimissüsteemi protrombootiline seisund.
7. endoteeli düsfunktsioon, mida iseloomustab plasminogeeni inhibiitori aktivaatori ja rakuadhesioonimolekulide suurenenud ekspressioon.
8. oksüdatiivne stress, mis põhjustab oksüdeeritud LDL-i ja F2-isoprostaanide kontsentratsiooni suurenemist.
9. süsteemne põletik, mille puhul suureneb fibrinogeeni ja C-reaktiivse valgu ekspressioon.
Kõige olulisemad riskitegurid koronaararterite haiguse tekkeks DM-2 puhul on kõrgenenud LDL, madal HDL, arteriaalne hüpertensioon, hüperglükeemia ja suitsetamine. Üks erinevusi DM-i aterosklerootilise protsessi vahel on levinum ja oklusiivse kahjustuse distaalne olemus, need. Sageli on protsessi kaasatud suhteliselt väiksemad arterid, mis raskendab kirurgilist ravi ja halvendab prognoosi.
Epidemioloogia
Risk haigestuda koronaartõve II tüüpi diabeediga inimestel on 6 korda suurem kui diabeedita inimestel, samas kui meestel ja naistel on see sama. Arteriaalne hüpertensioon tuvastatakse 20% DM-1 ja 75% DM-2 patsientidest. Üldiselt esineb seda DM-ga patsientidel kaks korda sagedamini kui neil, kellel seda ei esine. Perifeersete veresoonte oblitereeriv ateroskleroos areneb 10% DM-ga patsientidest. Ajuveresoonte trombemboolia areneb 8% diabeediga patsientidest (2-4 korda sagedamini kui diabeedita inimestel).
Kliinilised ilmingud
Põhimõtteliselt ei erine DM-ita isikute omadest. DM-2 kliinilises pildis tulevad sageli esile makrovaskulaarsed tüsistused (müokardiinfarkt, insult, jalgade veresoonte oklusiivne kahjustus) ja just nende arengu ajal avastatakse patsiendil sageli hüperglükeemia. Võib-olla kaasuva autonoomse neuropaatia tõttu esineb kuni 30% diabeediga inimeste müokardiinfarktidest ilma tüüpilise stenokardiahoota (valutu infarkt).
Diagnostika
Ateroskleroosi tüsistuste (CHD, tserebrovaskulaarne õnnetus, jalaarterite oklusiivsed kahjustused) diagnoosimise põhimõtted ei erine DM-ita isikute omadest. Mõõtmine vererõhk(BP) tuleks läbi viia igal diabeediga patsiendi arstivisiidil ja näitajate määramisel. lipiidide spekter vereanalüüs (üldkolesterool, triglütseriidid, LDL, HDL) diabeedi korral tuleks läbi viia vähemalt kord aastas.
Diferentsiaaldiagnoos
Muud südame-veresoonkonna haigused, sümptomaatiline arteriaalne hüpertensioon, sekundaarne düslipideemia.
Ravi
♦ Vererõhu kontroll. Süstoolse vererõhu õige tase diabeedi korral on alla 130 mmHg ja diastoolne 80 mmHg (tabel 7.3). Enamik patsiente vajab selle eesmärgi saavutamiseks mitut antihüpertensiivset ravimit. Diabeedi antihüpertensiivse ravi valikravimid on AKE inhibiitorid ja angiotensiini retseptori blokaatorid, millele vajadusel lisatakse tiasiiddiureetikume. Müokardiinfarkti põdenud diabeedihaigete valikravimid on β-blokaatorid.
♦ Düslipideemia korrigeerimine. Lipiidide spektri indikaatorite sihttasemed on esitatud tabelis. 7.3. Lipiidide taset langetava ravi valikravimid on 3-hüdroksü-3-metüülglutarüül-CoA reduktaasi (statiinid) inhibiitorid.
♦ trombotsüütidevastane ravi. Ravi aspiriiniga (75-100 mg/päevas) on näidustatud üle 40-aastastele diabeediga patsientidele, kellel on suurenenud risk haigestuda südame-veresoonkonna haigustesse (tüsistunud perekonna ajalugu, arteriaalne hüpertensioon, suitsetamine, düslipideemia, mikroalbuminuuria), samuti kõigile patsientidele. ateroskleroosi kliiniliste ilmingutega sekundaarse ennetusena.
♦ Koronaararterite haiguse skriinimine ja ravi. Koronaararterite haiguse välistamiseks mõeldud stressitestid on näidustatud südame-veresoonkonna haiguste sümptomitega patsientidele, samuti patoloogia avastamiseks EKG-s.
Prognoos
75% DM-2 ja 35% DM-1 patsientidest sureb südame-veresoonkonna haigustesse. Ligikaudu 50% II tüüpi diabeediga patsientidest sureb koronaararterite haiguse tüsistuste tõttu, 15% aju trombemboolia tõttu. Diabeedihaigete suremus müokardiinfarkti ületab 50%.
7.8.2. diabeetiline retinopaatia
diabeetiline retinopaatia(DR) - võrkkesta veresoonte mikroangiopaatia, mida iseloomustab mikroaneurüsmide, hemorraagiate, eksudatiivsete muutuste ja äsja moodustunud veresoonte vohamine, mis põhjustab osalist või täielikku nägemise kaotust (tabel 7.17).
Etioloogia
DR-i arengu peamine etioloogiline tegur on krooniline hüperglükeemia. Muud tegurid (arteriaalne hüpertensioon, düslipideemia, suitsetamine, rasedus jne) on vähem olulised.
Patogenees
DR-i patogeneesi peamised lingid on:
Võrkkesta veresoonte mikroangiopaatia, mis põhjustab veresoonte luumenuse ahenemist hüpoperfusiooni tekkega;
Laevade degeneratsioon koos mikroaneurüsmide moodustumisega;
Progresseeruv hüpoksia, mis stimuleerib veresoonte proliferatsiooni ja põhjustab rasvade degeneratsiooni ja kaltsiumisoolade ladestumist võrkkestas;
Tab. 7.17. diabeetiline retinopaatia
 eksudatsiooniga mikroinfarktid, mis põhjustavad pehmete "puuvillalaikude" moodustumist;
eksudatsiooniga mikroinfarktid, mis põhjustavad pehmete "puuvillalaikude" moodustumist;
Lipiidide ladestumine koos tihedate eksudaatide moodustumisega;
Paljunevate veresoonte kasv võrkkestas koos šuntide ja aneurüsmide moodustumisega, mis põhjustab veenide laienemist ja võrkkesta hüpoperfusiooni süvenemist;
Varastamise nähtus koos isheemia edasise progresseerumisega, mis on infiltraatide ja armide moodustumise põhjus;
Võrkkesta eraldumine selle isheemilise lagunemise ja klaaskesta tõmbe moodustumise tagajärjel;
Klaaskeha hemorraagia hemorraagilise infarkti, ulatusliku veresoonte invasiooni ja aneurüsmi rebendi tagajärjel;
Iirise veresoonte proliferatsioon (diabeetiline rubeoos), mis viib sekundaarse glaukoomi tekkeni;
Makulopaatia võrkkesta tursega.
Epidemioloogia
DR on arenenud riikide tööealise elanikkonna seas kõige levinum pimedaks jäämise põhjus ning DM-ga patsientidel on pimedaks jäämise risk 10-20 korda suurem kui üldpopulatsioonil. DM-1 diagnoosimise ajal ei leitud DR-i peaaegu ühelgi patsiendil, 5 aasta pärast avastatakse haigus 8% patsientidest ja 30-aastase diabeediga patsientidest - 98% patsientidest. CD-2 diagnoosimise ajal tuvastatakse DR 20–40% patsientidest ja 15-aastase CD-2 kogemusega patsientide hulgas 85%. SD-1 puhul on suhteliselt sagedasem proliferatiivne retinopaatia ja SD-2 puhul makulopaatia (75% makulopaatia juhtudest).
Kliinilised ilmingud
Üldtunnustatud klassifikatsiooni kohaselt on DR-i 3 etappi
(Tabel 7.18).
Diagnostika
Täielik oftalmoloogiline uuring, sealhulgas otsene oftalmoskoopia koos võrkkesta pildistamisega, on näidustatud DM-1-ga patsientidele 3-5 aastat pärast haiguse algust ja DM-2-ga patsientidele kohe pärast selle avastamist. Edaspidi tuleks selliseid uuringuid korrata igal aastal.
Tab. 7.18. Diabeetilise retinopaatia klassifikatsioon
 Diferentsiaaldiagnoos
Diferentsiaaldiagnoos
Muud silmahaigused diabeediga patsientidel.
Ravi
Diabeetilise retinopaatia, aga ka teiste hiliste tüsistuste ravi põhiprintsiip on DM optimaalne kompensatsioon. Kõige tõhusam diabeetilise retinopaatia ravi ja pimeduse ennetamine on laser fotokoagulatsioon. eesmärk
 Riis. 7.11. Diabeetiline retinopaatia:
Riis. 7.11. Diabeetiline retinopaatia:
a) leviku tõkestamine; b) preproliferatiivne; c) proliferatiivne
laserfotokoagulatsioon on äsja moodustunud veresoonte toimimise lõpetamine, mis kujutavad endast peamist ohtu selliste tõsiste tüsistuste tekkele nagu hemoftalmia, võrkkesta tõmbe irdumine, iirise rubeoos ja sekundaarne glaukoom.
Prognoos
Pimedus registreeritakse 2% DM-ga patsientidest (3-4% DM-1-ga patsientidest ja 1,5-2% DM-2-ga patsientidest). DR-iga seotud uute pimedaksjäämise juhtude ligikaudne määr on 3,3 juhtu 100 000 elaniku kohta aastas. DM-1 korral põhjustab HbA1c langus 7,0% -ni DR-i väljakujunemise riski vähenemise 75% ja DR-i progresseerumise riski vähenemise 60% võrra. DM-2 korral vähendab HbA1c 1% võrra DR-i tekke riski 20%.
7.8.3. diabeetiline nefropaatia
diabeetiline nefropaatia(DNF) on defineeritud kui albuminuuria (rohkem kui 300 mg albumiini päevas või proteinuuria üle 0,5 g valgu päevas) ja/või neerude filtreerimisfunktsiooni langus diabeediga inimestel kuseteede infektsioonide puudumisel. , südamepuudulikkus või muud neeruhaigused. Mikroalbuminuuria on defineeritud kui albumiini eritumine 30–300 mg/päevas või 20–200 mcg/min.
Etioloogia ja patogenees
DNF-i peamised riskitegurid on diabeedi kestus, krooniline hüperglükeemia, arteriaalne hüpertensioon, düslipideemia ja neeruhaigus vanematel. DNF-is mõjutab see peamiselt glomerulaaraparaat neerud.
1. Üks võimalikest mehhanismidest, mille abil hüperglükeemia aitab kaasa glomerulaarsete kahjustuste tekkele, on sorbitooli akumuleerumine glükoosi metabolismi polüooliraja aktiveerimise tõttu, samuti mitmed arenenud glükoosi lõpp-produktid.
2. Hemodünaamilised häired, nimelt intraglomerulaarne arteriaalne hüpertensioon(kõrgenenud vererõhk neeru glomerulites) on patogeneesi oluline komponent
Intraglomerulaarse hüpertensiooni põhjuseks on arterioolide tooni rikkumine: aferendi laienemine ja efferendi kitsenemine.
Tab. 7.19. diabeetiline nefropaatia
 See omakorda toimub mitmete humoraalsete tegurite, nagu angiotensiin-2 ja endoteliin, mõjul, samuti glomerulaarmembraani elektrolüütide omaduste rikkumise tõttu. Lisaks soodustab süsteemne hüpertensioon intraglomerulaarset hüpertensiooni, mis esineb enamikul DNF-ga patsientidel. Intraglomerulaarse hüpertensiooni tõttu kahjustuvad basaalmembraanid ja filtratsioonipoorid,
See omakorda toimub mitmete humoraalsete tegurite, nagu angiotensiin-2 ja endoteliin, mõjul, samuti glomerulaarmembraani elektrolüütide omaduste rikkumise tõttu. Lisaks soodustab süsteemne hüpertensioon intraglomerulaarset hüpertensiooni, mis esineb enamikul DNF-ga patsientidel. Intraglomerulaarse hüpertensiooni tõttu kahjustuvad basaalmembraanid ja filtratsioonipoorid,
mille kaudu hakkavad tungima jäljed (mikroalbuminuuria), millele järgneb märkimisväärne kogus albumiini (proteinuuria). Basaalmembraanide paksenemine põhjustab nende elektrolüütide omaduste muutumise, mis iseenesest viib selleni, et ultrafiltraati satub rohkem albumiini ka siis, kui filtratsioonipooride suurus ei muutu.
3. Geneetiline eelsoodumus. DNF-iga patsientide sugulastel esineb arteriaalne hüpertensioon sagedamini. On tõendeid seose kohta DNP ja ACE geeni polümorfismi vahel. Mikroskoopiliselt näitab DNF glomerulite basaalmembraanide paksenemist, mesangiumi laienemist, samuti fibrootilisi muutusi aferentsetes ja eferentsetes arterioolides. Viimases etapis, mis kliiniliselt vastab kroonilisele neerupuudulikkusele (CRF), määratakse fokaalne (Kimmelstiel-Wilson) ja seejärel difuusne glomeruloskleroos.
Epidemioloogia
Mikroalbuminuuria määratakse 6-60% DM-1-ga patsientidest 5-15 aastat pärast selle avaldumist. DNF määratakse 35%-l DM-1-ga patsientidest, sagedamini meestel ja neil, kellel tekkis DM-1 alla 15-aastaselt. DM-2-ga areneb DNF 25% Euroopa rassi ja 50% Aasia rassi esindajatest. Üldine DNF-i levimus T2DM-is on 4-30%.
Kliinilised ilmingud
Suhteliselt varajane kliiniline ilming, mis on kaudselt seotud DNF-iga, on arteriaalne hüpertensioon. Muud kliiniliselt ilmsed ilmingud on hilised. Nende hulka kuuluvad nefrootilise sündroomi ja kroonilise neerupuudulikkuse ilmingud.
Diagnostika
DNF-i sõelumine DM-iga inimestel hõlmab iga-aastast testimist mikroalbuminuuria DM-1-ga 5 aastat pärast haiguse ilmnemist ja DM-2-ga - kohe pärast selle avastamist. Lisaks on arvutamiseks vaja vähemalt kord aastas määrata kreatiniini taset glomerulaarfiltratsiooni kiirus (GFR). GFR-i saab arvutada erinevate valemitega, näiteks Cockcroft-Gault valemiga:
Meestel: a = 1,23 (GFR norm 100 - 150 ml/min) Naistel: a = 1,05 (GFR norm 85 - 130 ml/min)
DNF-i algstaadiumis võib tuvastada GFR-i tõusu, mis CRF-i edenedes järk-järgult langeb. Mikroalbuminuuriat hakatakse määrama 5-15 aastat pärast CD-1 avaldumist; DM-2 puhul tuvastatakse see 8-10% juhtudest kohe pärast avastamist, tõenäoliselt haiguse pika asümptomaatilise kulgemise tõttu enne diagnoosimist. T1DM-i ilmne proteinuuria või albuminuuria haripunkt saabub 15–20 aastat pärast tekkimist. Proteinuuria viitab pöördumatus DNF, mis varem või hiljem viib CRF-i. Ureemia tekib keskmiselt 7-10 aastat pärast ilmse proteinuuria tekkimist. Tuleb märkida, et GFR ei korreleeru proteinuuriaga.
Diferentsiaaldiagnoos
Muud proteinuuria ja neerupuudulikkuse põhjused diabeediga inimestel. Enamasti seostatakse DNF-i arteriaalse hüpertensiooni, diabeetilise retinopaatia või neuropaatiaga, mille puudumisel peaks diferentsiaaldiagnostika olema eriti ettevaatlik. 10% juhtudest DM-1 ja 30% juhtudest DM-2 puhul ei ole proteinuuria seotud DNP-ga.
Ravi
♦ Põhitingimused esmaseks ja sekundaarseks ärahoidmine
DNF on diabeedi kompenseerimine ja normaalse süsteemse arteriaalse rõhu säilitamine. Lisaks tähendab DNF-i esmane ennetamine valgu tarbimise vähendamist - vähem kui 35% päevastest kaloritest.
♦ Etapil mikroalbuminuuria Ja proteinuuria patsientidele näidatakse AKE inhibiitorite või angiotensiini retseptori blokaatorite määramist. Samaaegse arteriaalse hüpertensiooniga määratakse need antihüpertensiivsetes annustes, vajadusel kombinatsioonis teiste antihüpertensiivsete ravimitega. Normaalse vererõhu korral määratakse need ravimid annustes, mis ei põhjusta hüpotensiooni teket. Nii AKE inhibiitorid (DM-1 ja DM-2 puhul) kui ka angiotensiini retseptori blokaatorid (DM-2 puhul) aitavad vältida mikroalbuminuuria üleminekut proteinuuriaks. Mõnel juhul elimineeritakse mikroalbuminuuria selle ravi taustal koos diabeedi kompenseerimisega vastavalt muudele parameetritele. Lisaks on vajalik alates mikroalbuminuuria staadiumist
valgu tarbimise vähendamine alla 10% päevasest kalorikogusest (või alla 0,8 grammi kehakaalu kilogrammi kohta) ja soola tarbimise vähendamine alla 3 grammi päevas.
♦ Laval CKD, reeglina on vajalik hüpoglükeemilise ravi korrigeerimine. Enamik II tüüpi diabeediga patsiente tuleb üle viia insuliinravile, kuna TSP kuhjumisega kaasneb raske hüpoglükeemia tekke oht. Enamikul I tüüpi diabeediga patsientidel väheneb insuliinivajadus, kuna neerud on selle metabolismi üks peamisi kohti. Kui seerumi kreatiniinisisaldus tõuseb 500 µmol/l või rohkem, on vaja tõstatada küsimus patsiendi ettevalmistamisest kehaväliseks (hemodialüüs, peritoneaaldialüüs) või kirurgiliseks (neeru siirdamine) ravimeetodiks. Neerusiirdamine on näidustatud kreatiniinisisalduse korral kuni 600-700 µmol/l ja glomerulaarfiltratsiooni kiiruse vähenemise korral alla 25 ml/min, hemodialüüsi - vastavalt 1000-1200 µmol/l ja alla 10 ml/min.
Prognoos
50% 1. tüüpi diabeediga patsientidest ja 10% 2. tüüpi diabeediga patsientidest, kellel on proteinuuria, areneb krooniline neeruhaigus järgmise 10 aasta jooksul. 15% kõigist alla 50-aastaste I tüüpi diabeediga patsientide surmajuhtumitest on seotud DNP-st tingitud CRF-ga.
7.8.4. Diabeetiline neuropaatia
Diabeetiline neuropaatia(DNE) on närvisüsteemi kahjustuse sündroomide kombinatsioon, mida saab klassifitseerida sõltuvalt selle erinevate osakondade (sensoor-motoorne, autonoomne) valdavast osalusest protsessis, samuti kahjustuse levimusest ja raskusastmest ( Tabel 7.20).
I. Sensomotoorne neuropaatia:
sümmeetriline;
Fokaalne (mononeuropaatia) või polüfokaalne (kraniaalne, proksimaalne motoorne, jäsemete ja kehatüve mononeuropaatia).
II. Autonoomne (vegetatiivne) neuropaatia:
Kardiovaskulaarne (ortostaatiline hüpotensioon, südame denervatsiooni sündroom);
Seedetrakt (mao atoonia, sapiteede düskineesia, diabeetiline enteropaatia);
Urogenitaalne (koos põie- ja seksuaalfunktsiooni häiretega);
Patsiendi hüpoglükeemia äratundmise võime halvenemine;
Pupillide funktsiooni kahjustus;
Higinäärmete funktsioonide rikkumine (distaalne anhidroos, liighigistamine söömisel).
Tab. 7.20. Diabeetiline neuropaatia
 Etioloogia ja patogenees
Etioloogia ja patogenees
DNE peamine põhjus on hüperglükeemia. Selle patogeneesiks on välja pakutud mitmeid mehhanisme:
Glükoosi metabolismi polüooliraja aktiveerimine, mille tulemuseks on sorbitooli ja fruktoosi akumuleerumine närvirakkudes ning müoinositooli ja glutatiooni sisalduse vähenemine. See omakorda toob kaasa vabade radikaalide protsesside aktiveerumise ja lämmastikoksiidi taseme languse;
Närvirakkude membraani ja tsütoplasmaatiliste valkude mitteensümaatiline glükosüülimine;
Mikroangiopaatia vasa nervorum, mis põhjustab kapillaaride verevoolu aeglustumist ja närvide hüpoksiat.
Epidemioloogia
DNE levimus mõlemas DM-i tüübis on umbes 30%. DM-1 korral hakatakse seda 5 aasta pärast haiguse algusest tuvastama 10% patsientidest. Uute DNE juhtude sagedus DM-2 puhul on umbes 6% patsientidest aastas. Kõige tavalisem variant on distaalne sümmeetriline sensomotoorne NNE.
Kliinilised ilmingud
Sensorimootor DNE avaldub motoorsete ja sensoorsete häirete kompleksina. DNE distaalse vormi tavaline sümptom on paresteesia, mis väljenduvad "roomamistundes", tuimuses. Patsiendid kurdavad sageli külmade jalgade üle, kuigi need jäävad katsudes soojaks, mis on märk, mis eristab polüneuropaatiat isheemilistest muutustest, kui jalad on puudutamisel külmad. Vibratsioonitundlikkus on sensoorse neuropaatia varajane ilming. Iseloomulik on "rahutute jalgade" sündroom, mis on öise paresteesia ja ülitundlikkuse kombinatsioon. Valu jalgades sagedamini häiritakse öösel, samas kui mõnikord ei talu patsient teki puudutust. Tüüpilisel juhul võib valu, erinevalt arterite hävitavatest haigustest, leevendada kõndimisega. Aastaid hiljem võib valu spontaanselt lakata valutundlikkuse eest vastutavate väikeste närvikiudude surma tõttu. Hüpoesteesia mis väljendub "sukade" ja "kinnaste" tüüpide tundlikkuse kaotuses. Sügava propriotseptiivse tundlikkuse rikkumine põhjustab koordinatsiooni halvenemist ja liikumisraskusi (sensoorne ataksia). Patsient kaebab "kellegi teise jalgade" pärast, "vati peal seismise" tunnet. Troofilise innervatsiooni rikkumine põhjustab degeneratiivseid muutusi nahas, luudes ja kõõlustes. Valutundlikkuse rikkumine põhjustab jalgade sagedasi, patsiendile märkamatuid mikrotraumasid, mis on kergesti nakatunud. Koordinatsiooni ja kõndimise rikkumine põhjustab jala liigeste koormuse mittefüsioloogilist ümberjaotamist. Selle tulemusena on jala luu-lihassüsteemi anatoomilised suhted häiritud.
Jalavõlvi deformeerub, tursed, luumurrud, tekivad kroonilised mädased protsessid (vt punkt 7.8.5).
On mitmeid autonoomse DNE vorme. Põhjus kardiovaskulaarne vorm- südame-kopsukompleksi ja suurte veresoonte innervatsiooni rikkumine. Vagusnärv on pikim närv ja seetõttu mõjutab see varem kui teised. Sümpaatiliste mõjutuste ülekaalu tulemusena areneb rahuoleku tahhükardia. Ebapiisav reaktsioon ortostaasile avaldub ortostaatiline hüpotensioon ja minestus. Kopsu-südame kompleksi autonoomne denervatsioon viib südame löögisageduse varieeruvuse puudumiseni. Valutu müokardiinfarkti suurenenud esinemissagedus diabeediga patsientide seas on seotud autonoomse neuropaatiaga.
Sümptomid seedetrakti vorm DNE-d on gastroparees koos hilinenud või vastupidi kiire mao tühjenemisega, mis võib tekitada raskusi insuliinravi valikul, kuna süsivesikute imendumise aeg ja maht varieeruvad määramatult; söögitoru atoonia, refluksösofagiit, düsfaagia; vesine kõhulahtisus. Sest urogenitaalne vorm DNE-d iseloomustab kusejuhade ja põie atoonia, mis põhjustab kalduvust kuseteede infektsioonidele; erektsioonihäired (umbes 50% diabeediga patsientidest); retrograadne ejakulatsioon.
Teised autonoomse DNE võimalikud ilmingud on halvenenud võime ära tunda hüpoglükeemiat, pupillide funktsiooni kahjustus, higinäärmete funktsiooni kahjustus (anhidroos) ja diabeetiline amüotroofia.
Diagnostika
DM-ga patsientide neuroloogiline läbivaatus tuleb läbi viia igal aastal. See hõlmab vähemalt testimist distaalse sensomotoorse neuropaatia tuvastamiseks. Selleks hinnatakse vibratsioonitundlikkust gradueeritud häälekahvli abil, puutetundlikkust monofilamendi abil, samuti temperatuuri- ja valutundlikkust. Vastavalt näidustustele uuritakse autonoomse närvisüsteemi seisundit: südame parasümpaatilise innervatsiooni puudulikkuse diagnoosimiseks kasutatakse mitmeid funktsionaalseid teste, näiteks südame löögisageduse mõõtmist sügaval hingamisel koos varieeruvuse hindamisega.
pulsisagedus ja Valsalva test; ortostaatilist testi kasutatakse südame sümpaatilise innervatsiooni puudulikkuse diagnoosimiseks.
Diferentsiaaldiagnoos
Muu päritolu neuropaatia (alkohoolne, ureemiline, B 12 vaegusaneemiaga jne). Autonoomse neuropaatia tagajärjel tekkinud ühe või teise organi düsfunktsiooni diagnoos pannakse paika alles pärast elundipatoloogia välistamist.
Ravi
1. Hüpoglükeemilise ravi optimeerimine.
2. Jalgade hooldus (vt punkt 7.8.5).
3. Neurotroopsete ravimite (α-lipoehape) efektiivsust ei kinnitata kõigis uuringutes.
4. Sümptomaatiline ravi (valu vaigistamine, sildenafiil erektsioonihäirete korral, fludrokortisoon ortostaatilise hüpotensiooni korral jne).
Prognoos
Algstaadiumis võib DNE olla pöörduv DM stabiilse kompenseerimise taustal. DNE määratakse 80% haavanditega patsientidest ja see on jala amputatsiooni peamine riskitegur.
7.8.5. diabeetilise jala sündroom
diabeetilise jala sündroom(SDS) - jala patoloogiline seisund DM-s, mis tekib perifeersete närvide, naha ja pehmete kudede, luude ja liigeste kahjustuse taustal ning avaldub ägedate ja krooniliste haavandite, osteoartikulaarsete kahjustuste ja mädaste nekrootiliste protsessidena (tabel 7.21). .
Etioloogia ja patogenees
DFS-i patogenees on mitmekomponentne ja seda esindab neuropaatiliste ja perfusioonihäirete kombinatsioon, millel on väljendunud kalduvus infektsioonidele. Lähtudes ühe või teise loetletud teguri ülekaalust patogeneesis, eristatakse 3 peamist vormi
Tab. 7.21. diabeetilise jala sündroom
 I. Neuropaatiline vorm(60-70 %):
I. Neuropaatiline vorm(60-70 %):
Ilma osteoartropaatiata;
diabeetilise osteoartropaatiaga.
II. Neuroisheemia (segatud) vorm(15-20 %).
III. Isheemiline vorm(3-7 %).
SDS neuropaatiline vorm. Diabeetilise neuropaatia korral on kahjustatud peamiselt pikimate närvide distaalsed osad. Troofiliste impulsside pikaajaline defitsiit põhjustab naha, luude, sidemete, kõõluste ja lihaste hüpotroofiat. Sidestruktuuride hüpotroofia tagajärjeks on jala deformeerumine koos tugikoormuse mittefüsioloogilise ümberjaotusega ja selle ülemäärane suurenemine teatud piirkondades. Nendes kohtades, näiteks metatarsaalsete luude peade projektsioonis, täheldatakse naha paksenemist ja hüperkeratoosi teket. Pidev surve nendele piirkondadele viib aluseks olevate pehmete kudede põletikulise autolüüsini, mis loob eeldused haavandi tekkeks. Atroofia ja nõrgenenud higistamise tagajärjel muutub nahk kuivaks ja kergesti lõhenevaks. Valutundlikkuse vähenemise tõttu ei pööra patsient sageli toimuvatele muutustele tähelepanu. Ta ei suuda õigeaegselt tuvastada kingade ebamugavust, mis põhjustab kriimustuste ja kalluste moodustumist, ei märka võõrkehade sissetoomist, väikseid haavu pragunemise kohtadesse. Olukorda süvendab sügava tundlikkuse rikkumine, mis väljendub kõnnaku rikkumises, jala vales paigaldamises. Kõige sagedamini on peptiline haavand nakatunud stafülokokkide, streptokokkide, soolestiku rühma bakteritega; anaeroobne taimestik liitub sageli. Neuropaatiline osteoartropaatia on jala osteoartikulaarse aparatuuri väljendunud düstroofsete muutuste (osteoporoos, osteolüüs, hüperostoos) tagajärg.
SDS-i isheemiline vorm on alajäsemete arterite ateroskleroosi tagajärg, mis viib peamise verevoolu rikkumiseni, st. on üks diabeetilise makroangiopaatia variante.
Epidemioloogia
SDS-i täheldatakse 10-25% -l ja teatud andmetel ühel või teisel kujul 30-80% diabeediga patsientidest. Ameerika Ühendriikides on DFS-iga diabeedihaigete ravi aastased kulud 1 miljard dollarit.
Kliinilised ilmingud
Kell neuropaatiline vorm SDS eristab kahte kõige levinumat tüüpi kahjustusi: neuropaatiline haavand ja osteoartropaatia (koos arenguga
 Riis. 7.12. Neuropaatiline haavand diabeetilise jala sündroomi korral
Riis. 7.12. Neuropaatiline haavand diabeetilise jala sündroomi korral
 Riis. 7.13. Charcoti liiges diabeetilise jala sündroomi korral
Riis. 7.13. Charcoti liiges diabeetilise jala sündroomi korral
Charcot liigend). neuropaatilised haavandid, reeglina paiknevad need talla- ja sõrmedevaheliste ruumide piirkonnas, st. jalalaba piirkondadele, mis kogevad suurimat survet (joonis 7.12).
Destruktiivsed muutused jala luus ja sidemetes võivad areneda mitme kuu jooksul ja põhjustada luude tõsist deformatsiooni - diabeetiline osteoartropaatia ja moodustamine puuliige, samal ajal võrreldakse jalga piltlikult "kondikotiga"
Kell SDS isheemiline vorm
jalgade nahk on külm, kahvatu või tsüanootiline; harva on roosakas-punane toon, mis on tingitud pindmiste kapillaaride laienemisest vastusena isheemiale. Haavandilised defektid tekivad akraalse nekroosina – sõrmeotstel, kandade äärepinnal (joon. 7.14).
Pulss jalalaba arteritel, popliteaal- ja reieluuarteritel on nõrgenenud või ei ole palpeeritav.
Tüüpilistel juhtudel kurdavad patsiendid "vahelduvat lonkamist". Jäseme isheemilise kahjustuse raskusastme määravad kolm peamist tegurit: stenoosi raskusaste, kollateraalse verevoolu areng, vere hüübimissüsteemi seisund.
Diagnostika
Diabeedihaige jalgu tuleks kontrollida iga kord arstivisiidi ajal, vähemalt kord poole aasta jooksul. SDS-i diagnoos hõlmab:
 Riis. 7.14. Akranekroos diabeetilise jala sündroomi isheemilises vormis
Riis. 7.14. Akranekroos diabeetilise jala sündroomi isheemilises vormis
Jalgade uurimine;
Neuroloogilise seisundi hindamine - erinevat tüüpi tundlikkus, kõõluste refleksid, elektromüograafia;
Arteriaalse verevoolu seisundi hindamine - angiograafia, dopplerograafia, dopplerograafia;
jalgade ja pahkluude röntgenuuring;
Haavavooluse bakterioloogiline uuring.
Diferentsiaaldiagnoos
See viiakse läbi erineva päritoluga jalgade haavaprotsesside, samuti muude alajäsemete veresoonte oklusiivsete haiguste ja jala liigeste patoloogiaga. Lisaks on vaja eristada SDS-i kliinilisi vorme (tabel 7.22).
Ravi
Ravi neuropaatiliselt nakatunud VTS-vormid sisaldavad järgmisi tegevusi:
DM-i kompenseerimise optimeerimine, reeglina insuliini annuse suurendamine ja DM-2 korral - sellele ülekandmine;
süsteemne antibiootikumravi;
jala täielik mahalaadimine (see võib viia aastaid eksisteerinud haavandite paranemiseni mõne nädala jooksul);
Haava lokaalne ravi hüperkeratoosi piirkondade eemaldamisega;
Jalgade hooldus, õige valik ja spetsiaalsete jalanõude kandmine. Õigeaegne konservatiivne ravi võimaldab
vältida operatsiooni 95% juhtudest.
Tab. 7.22. SDS-i kliiniliste vormide diferentsiaaldiagnostika
 Ravi isheemiline VTS-vormid hõlmavad järgmist:
Ravi isheemiline VTS-vormid hõlmavad järgmist:
DM-i kompenseerimise optimeerimine, reeglina insuliini annuse suurendamine ja DM-2 korral - sellele ülekandmine;
Haavandiliste-nekrootiliste kahjustuste puudumisel tegevusteraapia (1-2-tunnine jalutuskäik päevas, mis aitab kaasa kollateraalse verevoolu arengule);
kahjustatud veresoonted;
Konservatiivne ravi: antikoagulandid, aspiriin (kuni 100 mg / päevas), vajadusel - fibrinolüütikumid, prostaglandiin E1 ja prostatsükliini preparaadid.
Ulatusliku mäda-nekrootilise kahjustuse tekkimisega kõigis SDS-i variantides tõstatatakse amputatsiooni küsimus.
Prognoos
50–70% teostatud jala amputatsioonide koguarvust on DM patsientidel. Jalgade amputatsioonid on diabeetikutel 20–40 korda sagedasemad kui mittediabeetilistel patsientidel.
7.9. DIABEED JA RASEDUS
Rasedusdiabeet(GDM) on glükoositalumatus, mis tuvastati esmakordselt raseduse ajal (tabel 7.23). See määratlus ei välista võimalust, et süsivesikute ainevahetuse patoloogia võib eelneda rasedusele. GDM-i tuleks eristada olukordadest, kus varem diagnoositud diabeediga naine (vanuse tõttu sagedamini 1. tüüpi diabeet) rasestub.
Etioloogia ja patogenees
GDM-iga on need sarnased SD-2-ga. Munasarjade ja platsenta steroidide kõrge tase, samuti kortisooli moodustumise suurenemine neerupealiste koores põhjustavad raseduse ajal füsioloogilise insuliiniresistentsuse kujunemist. GDM-i teket seostatakse asjaoluga, et raseduse ajal loomulikult tekkiv insuliiniresistentsus ja sellest tulenevalt eelsoodumusega isikute suurenenud insuliinivajadus ületab pankrease β-rakkude funktsionaalset võimekust. Pärast sünnitust, hormonaalsete ja metaboolsete suhete taastumisega algtasemele, see tavaliselt kaob.
Tab. 7.23. Rasedusdiabeet
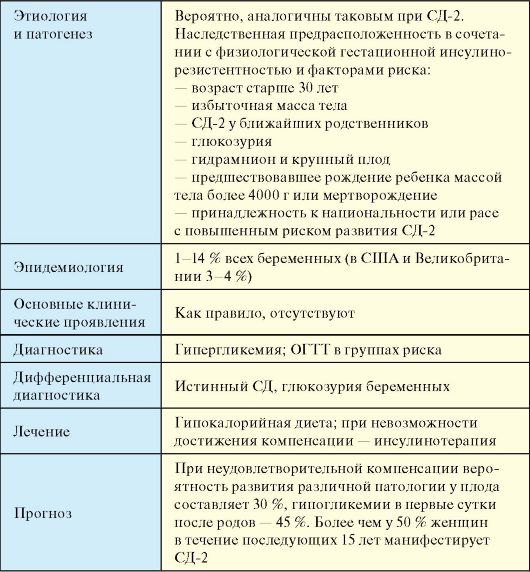 GDM areneb tavaliselt 2. trimestri keskel, raseduse 4. ja 8. kuu vahel. Enamikul patsientidest on liigne kehakaal ja CD-2 anamnees on koormatud. GDM-i väljakujunemise riskitegurid, samuti naiste rühmad, kellel on madal risk GDM-i tekkeks, on toodud tabelis. 7.24.
GDM areneb tavaliselt 2. trimestri keskel, raseduse 4. ja 8. kuu vahel. Enamikul patsientidest on liigne kehakaal ja CD-2 anamnees on koormatud. GDM-i väljakujunemise riskitegurid, samuti naiste rühmad, kellel on madal risk GDM-i tekkeks, on toodud tabelis. 7.24.
Tab. 7.24. Rasedusdiabeedi riskifaktorid
 Ema hüperglükeemia põhjustab lapse vereringesüsteemi hüperglükeemiat. Glükoos läbib kergesti platsentat ja läheb pidevalt ema verest lootele. Samuti toimub aktiivne aminohapete transport ja ketokehade ülekandumine lootele. Seevastu insuliin, glükagoon ja emalt saadud vabad rasvhapped ei satu loote verre. Esimesel 9-12 rasedusnädalal ei tooda loote kõhunääre veel oma insuliini. See aeg vastab loote organogeneesi faasile, mil pideva hüperglükeemia korral võivad emal tekkida mitmesugused väärarengud (süda, selg, seljaaju, seedetrakt). Alates 12. rasedusnädalast hakkab loote kõhunääre sünteesima insuliini ning vastusena hüperglükeemiale areneb loote pankrease β-rakkude reaktiivne hüpertroofia ja hüperplaasia. Hüperinsulineemia tõttu areneb loote makrosoomia, aga ka letsitiini sünteesi pärssimine, mis seletab vastsündinute respiratoorse distressi sündroomi suurt esinemissagedust. β-rakkude hüperplaasia ja hüperinsulinemia tagajärjel on kalduvus raskele ja pikaajalisele hüpoglükeemiale.
Ema hüperglükeemia põhjustab lapse vereringesüsteemi hüperglükeemiat. Glükoos läbib kergesti platsentat ja läheb pidevalt ema verest lootele. Samuti toimub aktiivne aminohapete transport ja ketokehade ülekandumine lootele. Seevastu insuliin, glükagoon ja emalt saadud vabad rasvhapped ei satu loote verre. Esimesel 9-12 rasedusnädalal ei tooda loote kõhunääre veel oma insuliini. See aeg vastab loote organogeneesi faasile, mil pideva hüperglükeemia korral võivad emal tekkida mitmesugused väärarengud (süda, selg, seljaaju, seedetrakt). Alates 12. rasedusnädalast hakkab loote kõhunääre sünteesima insuliini ning vastusena hüperglükeemiale areneb loote pankrease β-rakkude reaktiivne hüpertroofia ja hüperplaasia. Hüperinsulineemia tõttu areneb loote makrosoomia, aga ka letsitiini sünteesi pärssimine, mis seletab vastsündinute respiratoorse distressi sündroomi suurt esinemissagedust. β-rakkude hüperplaasia ja hüperinsulinemia tagajärjel on kalduvus raskele ja pikaajalisele hüpoglükeemiale.
Epidemioloogia
DM mõjutab 0,3% kõigist reproduktiivses eas naistest, 0,2-0,3% rasedatest on juba alguses ja 1-14% rasedustest areneb GDM või ilmneb tõeline DM. GDM-i levimus on erinevates populatsioonides erinev, näiteks USA-s avastatakse seda ligikaudu 4% rasedatel (135 tuhat juhtu aastas).
Kliinilised ilmingud
GSD-s puudub. Võib esineda dekompenseeritud diabeedi mittespetsiifilisi sümptomeid.
Diagnostika
Tühja kõhu veresuhkru tase on biokeemilise vereanalüüsi osana näidustatud kõigile rasedatele naistele. Riskirühma kuuluvatel naistel (tabel 7.24) on näidatud suukaudne glükoositaluvuse test(OGTT). Kirjeldatakse paljusid selle rakendamise variante rasedatel naistel. Lihtsaim neist eeldab järgmisi reegleid:
3 päeva enne uuringut on naine tavapärasel dieedil ja järgib oma tavapärast füüsilist koormust;
Katse tehakse hommikul tühja kõhuga pärast vähemalt 8-tunnist üleöö paastumist;
Pärast tühja kõhuga vereproovi võtmist joob naine 5 minutit lahust, mis koosneb 75 grammist kuivast glükoosist, mis on lahustatud 250–300 ml vees; 2 tunni pärast tehakse korduv glükeemia taseme määramine.
GDM-i diagnoos põhineb järgmisel kriteeriumid:
Täisvere (venoosne, kapillaar) glükoos tühja kõhuga > 6,1 mmol/l või
Venoosse plasma glükoosisisaldus ≥ 7 mmol/l või
Glükoos kapillaari täisveres või venoosses plasmas 2 tundi pärast 75 g glükoosi ≥ 7,8 mmol/l manustamist.
Kui riskirühma kuuluval naisel on uuringu tulemused normaalsed, korratakse testi 24-28 rasedusnädalal.
Diferentsiaaldiagnoos
GSD ja tõeline SD; glükosuuria raseduse ajal.
Ravi
Risk emale ja lootele, samuti lähenemisviisid diabeedi ravile ja selle kontrolli tunnused GDM-i ja tõelise diabeedi korral on samad. Diabeedi hilised tüsistused raseduse ajal võivad märkimisväärselt edeneda, kuid kvaliteetse diabeedi kompenseerimise korral puuduvad raseduse katkemise näidustused. Diabeediga (tavaliselt DM-1) naine peaks rasedust planeerima noores eas, kui tüsistuste risk on kõige väiksem. Kui rasedus on planeeritud, on soovitatav rasedus katkestada.
vastuvõtt paar kuud pärast optimaalse hüvitise saavutamist. Raseduse planeerimise vastunäidustused on raskekujuline nefropaatia koos progresseeruva neerupuudulikkusega, raske südame isheemiatõbi, raskekujuline proliferatiivne retinopaatia, mida ei saa korrigeerida, ketoatsidoos raseduse alguses (ketoonkehad on teratogeensed tegurid).
Ravi eesmärk GDM ja tõeline diabeet raseduse ajal on järgmiste laboriparameetrite saavutamine:
tühja kõhuga glükoos< 5-5,8 ммоль/л;
Glükeemia 1 tund pärast söömist< 7,8 ммоль/л;
Glükeemia 2 tundi pärast söömist< 6,7 ммоль/л;
Keskmine päevane glükeemiline profiil< 5,5 ммоль/л;
HbA1c tase kuukontrollis, nagu tervetel inimestel (4-6%).
DM-1-ga, nagu ka väljaspool rasedust, peaks naine saama intensiivset insuliinravi, kuid raseduse ajal soovitatakse glükeemia taset hinnata 7-8 korda päevas. Kui tavapäraste süstide taustal ei ole võimalik normoglükeemilist kompensatsiooni saavutada, tuleb kaaluda patsiendi üleviimist insuliinravile, kasutades insuliini dosaatorit.
Esimesel etapil GDM-i ravi on ette nähtud dieetteraapia, mis seisneb päevase kalorite tarbimise piiramises umbes 25 kcal / kg tegelikust kaalust, seda eelkõige kergesti seeditavate loomset päritolu süsivesikute ja rasvade tõttu, samuti kehalise aktiivsuse suurendamise tõttu. Kui dieetravi taustal ei ole võimalik ravi eesmärke saavutada, tuleb patsiendile määrata intensiivne insuliinravi. Kõik tabletid diabeedivastased ravimid (TSP) raseduse ajal vastunäidustatud. Umbes 15% naistest tuleb üle viia insuliinravile.
Prognoos
GDM ja DM ebarahuldava kompenseerimise korral raseduse ajal on lootel erinevate patoloogiate tekke tõenäosus 30% (risk on 12 korda suurem kui üldpopulatsioonis). Rohkem kui 50% naistest, kellel tekib raseduse ajal GDM, tekib CD-2 järgmise 15 aasta jooksul.
